ბაქტერიები და ვირუსები
ნაწილი III – კორონავირუსები
ავტორი: ჯანო მარხულია (J. Markhulia )
The third part of the article series “Bacteria and Viruses” is entirely devoted to coronaviruses (CoVs). The reader will receive information about 7 currently known types of human coronavirus – HCoV. The taxonomy of coronaviruses, a chronology of their discovery, zoonotic origin, interspecific transmission and pathogenesis, structure, genome organization, penetration into the target cell, and replication cycle of CoVs are discussed. Current scientific strategies for combating the coronavirus are reviewed.
სტატიათა ციკლის „ბაქტერიები და ვირუსების“ მესამე ნაწილი (იხ. ნაწილი I — ბაქტერიები, ნაწილი II –ვირუსები) მთლიანად ეთმობა კორონავირუსებს. მკითხველი მიიღებს ინფორმაციას დღეისათვის, მეცნიერებისთვის ცნობილი, შვიდი სახეობის ადამიანის კორონავირუსის (HCoV – Human coronavirus) შესახებ. ყურადღება გამახვილებულია მათი აღმოჩენის ისტორიაზე, ზოონოზურ წარმომავლობაზე, სახეობათშორისო გადაცემაზე და ვირუსის რეპლიკაციაზე.
შესავალი
კორონავირუსული დაავადება 2019-მა, ან როგორც მას ხშირად მოიხსენიებენ – COVID-19 (coronavirus disease 19)-ის ეპიდემიამ, მსოფლიო მასშტაბით შექმნა უდიდესი სამედიცინო, სამეცნიერო, სოციალური და მორალური პრობლემა. მწვავე რესპირატორული დაავადება, რომელიც გამოწვეულია ახალი კორონავირუსით SARS-CoV-2-ით, ოფიციალური სახელწოდების მიღებამდე მოიხსენებოდა, როგორც „2019 წლის ახალი კორონავირუსი – novel coronavirus 2019 (2019-nCoV).
COVID-19 თავდაპირველად დაფიქსირდა ჩინეთში 2019 წლის ბოლოს, შემდეგ მან თანდათანობით მოიცვა მთელი მსოფლიო და გახდა გლობალური პანდემიის მიზეზი. ვირუსული ინფექცია დღემდე მძვინვარებს და განაგრძობს გავრცელებას. ამ ვირუსმა დააინფიცირა მილიონობით ადამიანი და გადაიქცა მთელი კაცობრიობის უმთავრეს გადასაწყვეტ პრობლემად.
COVID-19-ი წარმოადგენს ოცდამეერთე საუკუნის რიგით მესამე მაღალპათოგენურ და ყველაზე მსხვილმასშტაბიან კორონავირუსულ ეპიდემიას. 27.03.2021 მდგომარეობით დაავადების დადასტურებულ შემთხვევათა რიცხვმა შეადგენა 126,897,690 (გარდაცვლილთა რაოდენობა –2,782,548, ხოლო გამოჯანმრთელდა 102,305,833 ადამიანი).
SARS-CoV-2 ინფექცია იწვევს როგორც ზედა, ისე ქვედა სასუნთქი გზების დაზიანებას, ხოლო ადამიანიდან ადამიანზე გადაცემა ხდება დაინფიცირებულის აშკარა სიმპტომების გამოვლენამდეც. COVID-19-ით დაინფიცირებულ პაციენტთა კლინიკური გარეგნული ნიშანი მოიცავს ცხელებას, ხველას, სწრაფ დაღლილობას, ცალკეულ პაციენტებში კი გამოვლენილია კუჭ-ნაწლავური ინფექციის სიმპტომები. ხანდაზმულებსა და თანმდევი ქრონიკული დაავადებების მქონე ადამიანებში მეტია გავრცელებისა და გართულების შემთხვევათა ალბათობა [1].
ამჟამად, შემუშავებულია ვირუსთან ბრძოლის რამდენიმე ანტივირუსული სტრატეგია. ჯანდაცვის მსოფლიო ორგანიზაციის (ჯანმო) მიერ ნებადართულია სხვადასხვა წამყვანი ბიოსამედიცინო კომპანიის მიერ წარმოებული კოვიდსაწინააღმდეგო ვაქცინების გამოყენება, ასევე მიმდინარეობს გამოცდა ანტივირუსული და რეპროდუქციული წამლების ცალკეულ ძლიერ კანდიდატებზე.
სტატიათა ციკლის ამ ნაწილში განხილულია კორონავირუსების ტაქსონომია, ზოონოზური წარმომავლობა, სახეობათაშორისი გადაცემა და პათონოგენეზი, სტრუქტურა, გენომის ორგანიზაცია, ვირუსის სამიზნე უჯრედში შეღწევა და რეპლიკაციის ციკლი, ასევე COVID-19– ის ეპიდემიოლოგიის, კლინიკური მახასიათებლების უახლესი კვლევის მიმდინარეობა. მიმოხილულია კორონავირუსის წინააღმდეგ ბრძოლის მიმდინარე სამეცნიერო სტრატეგიები.
ვფიქრობთ, ვირუსებზე (ზოგადად) და კერძოდ კი ადამიანის კორონავირუსებზე საბაზისო ცოდნის მიღება მკითხველს შეუქმნის საერთო წარმოდგენას ამ ინფექციურ აგენტებზე და მისგან გამოწვეულ დაავადებებზე, ხელს შეუწყობს ჯანმრთელობის მსოფლიო ორგანიზაციის ინფექციისგან თავდაცვის რეკომენდაციების უკეთ გააზრებას და მის შესრულებას, რაც წარმოადგენს ეპიდემიის გავრცელების, შეზღუდვისა და მისი შეჩერების ერთ-ერთ უმთავრეს იარაღს.
1. კორონავირუსები
1.1 კლასიფიკაცია, ვირიონის მორფოლოგია და სტრუქტურული ცილები
კორონავირუსები (Coronaviruses – CoVs) განეკუთნება Coronaviridae – ვირუსების ოჯახს, ნიდოვირუსების (Nidovirales) რიგიდან (სურ. 1 – 3) [1-4].
Nidovirales რიგი აერთიანებს გარსიან რნმ-გენომის მქონე ვირუსებს, ხოლო საკუთრივ კორონავირუსები წარმოადგენენ ერთჯაჭვიან დადებით (+) რნმ – ვირუსებს [1]. სხვა ცნობილ რნმ-ვირუსებთან შედარებით მათ გააჩნიათ ყველაზე დიდი გენომი – გენომის სიგრძე მერყეობს 26,4-დან (შაშვის კორონავირუსი) – 31.7 (დღეისათვის ცნობილი ყელაზე დიდი – თეთრი ვეშაპის გამავირუსი gammacoronavirus ) კილობაზამდე (kbs). ვირიონების დიამეტრი გარსთან ერთად იცვლება 118–140 ნანომეტრმდე (ნმ) [2-8].
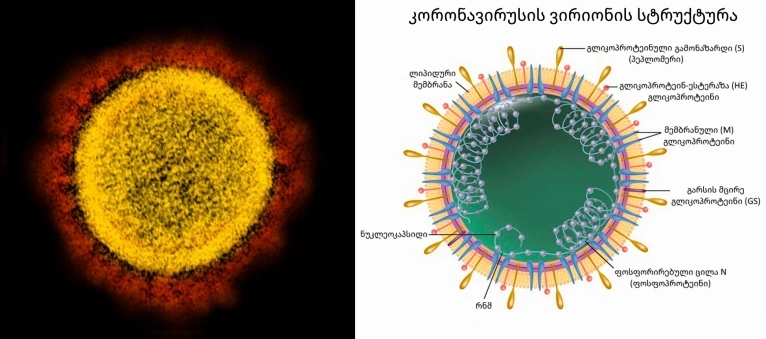
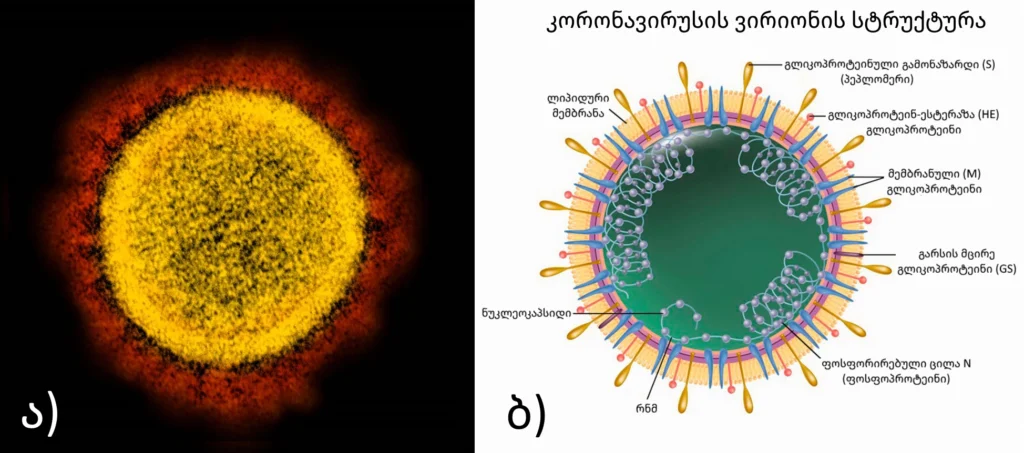
კრიოგენული ელექტრონული მიკროსკოპით გადაღებული ფოტოსურათების მიხედვით, კორონავირუსების ვირიონებს გააჩნიათ სფერული მორფოლოგია, რომლის გარშემო დაიმზირება 15-20 ნმ ზომის გლიკოპროტეინული გამონაზარდები (პეპლომერები), რის გამოც ვირუსული ნაწილაკები ემსგავსებიან მზის გვირგვინის – კორონას (corona) გამოსახულებას, სწორედ აქედან მომდინარეობს მათი სახელწოდებაც (ძველბერძნულად κορώνη (korṓnē )-გვირგვინი, ლათ. Corona) (სურ. 1 ა) [5-10].
კორონავირუსები იწვევენ რესპირატორულ და ნაწლავურ ინფექციებს ცხოველებსა და ადამიანებში [5-10].
კორონავირუსების გენომი მოთავსებულია სპირალურ კაფსიდში (სურ. 1 ბ), რომელიც წარმოქმნილია ნუკლეოკაფსიდური ცილისგან (N). ნუკლეოკაფსიდი თავის მხირვ შემოსაზღვრულია გარსით. ვირუსის გარსთან დაკავშირებულია მინიმუმ სამი სტრუქტურული ცილა: მემბრანული ცილა (M), გარსის ცილა (E) (იგივე (GS)) და გლიკოპროტეინული გამონაზარდი – ცილა (S) (ე.წ „სპაიკი“). M და E ცილები მონაწილეობს ვირუსის აწყობაში, მაშინ როდესაც გლიკოპროტეინული გამონაზარდი – S შუამავლობს ვირუსული ნაწილაკის მასპინძელ-უჯრედში შეღწევას. კორონავირუსების ცალკეულ სახეობებს ასევე გააჩნიათ გარსთან შეკავშირებული ჰემაგლუტინ-ესტერაზა ცილა (HE –hemagglutinin-esterase protein). ამ სტუქტურული ცილებიდან სწორედ “სპაიკები” (S -ცილები) ქმნიან ყველაზე დიდ გამონაზარდებს გარსზე [15-16].
[1] კორონავირუსების ერთჯაჭვიანი (+) რნმ, ფუნქციონირებს როგორც გენომი და როგორც მატრიცული რნმ (მ-რნმ). [7]
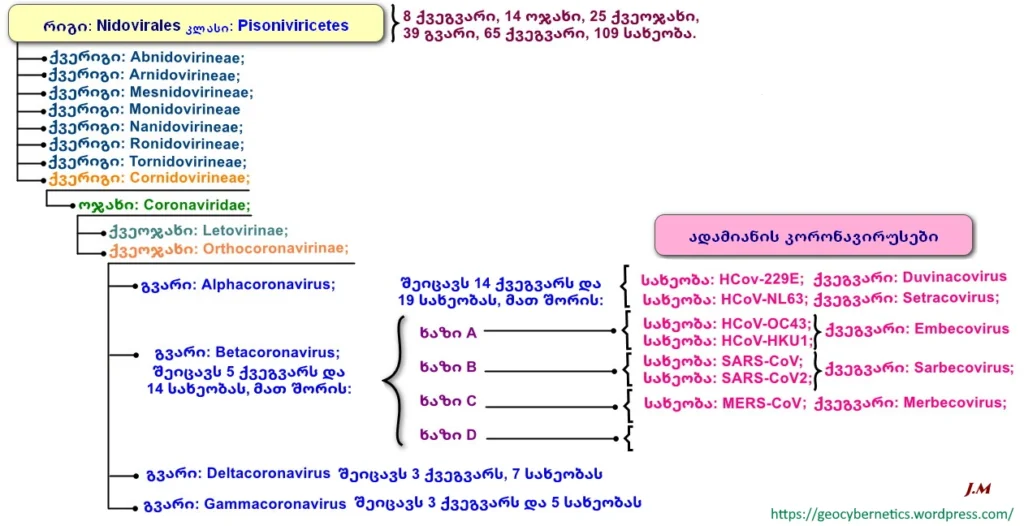
Nidovirales ვირუსების რიგი განსაზღვრული იქნა ვირუსების ტაქსონომიის საერთაშორისო კომიტეტის (ICTV) მიერ 1996 წელს. ვირუსების ტაქსონომიის 2019 წლის გამოცემის[2] (EC 51, Berlin, Germany, July 2019 Email ratification March 2020 (MSL #35)) მიხედვით ეს რიგი შეიცავს 8 ქვერიგს, 14 ოჯახს, 25 ქვეოჯახს, 39 გვარს, 65 ქვეგვარს და 109 სახეობას. თუ ამჟამინდელ კლასიფიკაციას შევადარებთ ვირუსების ტაქსონომიის 2017 წლის გამოცემას (EC 49, Singapore, July 2017
Email ratification 2018 (MSL #32) (MSL #32), რომლის მიხედვით ეს რიგი შეიცავდა ვირუსების 4 ოჯახს, 2 ქვეოჯახს, 13 გვარს და 64 სახეობას, თვალშისაცემია ის ცვლილება, რომელიც განიცადა ამ ორი წლის განმავლობაში მოცემული რიგის (ისევე როგორც მთლიანად) ვირუსების ტაქსონომიამ [17-19]. აღნიშნული კლასიფიკაცია დაფუძნებილია ვირუსილი გენომის ორგანიზაციაზე, გენომის მიმდევრობის მსგავსებაზე, ვირუსული ცილების ანტიგენურ თვისებებზე, რეპლიკაციის სტრატეგიაზე, ვირიონების სტრუქტურასა და ფიზიკურ-ქიმიურ თვისებებზე, მასპინძლის ბუნებრივ არეალზე, უჯრედულ და ქსოვილურ ტროპიზმე [18].
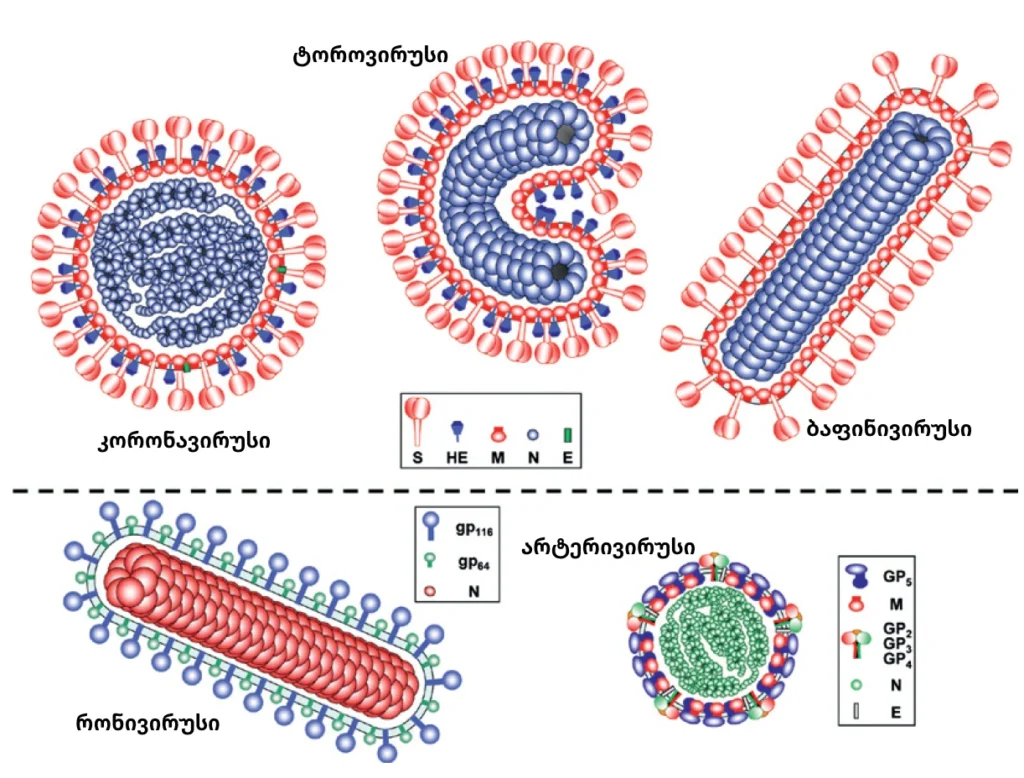
Nidovirales-ის რიგის მონოფილეტური კლასტერი – Coronaviridae ოჯახის წევრები, წარმოადგენენ ხერხემლიანთა სამი კლასის (ძუძუმწოვრები (კორონა და ტოპოვირუსები), ფრინველები (კორონავირუსები) და თევზები (ბაფინივირუსები)) ერთჯაჭვიან დადებით რნმ ვირუსებს [2].
სამივე კლასის ვირუსების ვირიონები, როგორც წესი, ერთმანეთისგან განსხვავდებიან მორფოლოგიით. კერძოდ, კორონავირუსების (Coronavirinae) ვირუსულ ნაწილაკებს, როგორც ავღნიშნეთ გააჩნიათ სფეროსებრი ფორმა ზომით – 120-160 ნმ. ბაფინივირუსების (Bafinivirus) ვირუსული ნაწილაკები ჩხირისებრია, ზომით – 70 – 200 × 75 – 88 ნმ. ასევე გვხდება ამ ორი ვარიანტის კომბინაციაც, მოხრილი ან ნახევარ მთვარისებრი ფორმების, მაგალითად ტოროვირუსები (Torovirus)[2,9-10,19].
[2] პირველი გამოცემა გამოქვეყნდა 1971 წელს.
1.1.1 ვირუსების Coronaviridae- ოჯახი
ვირუსების Coronaviridae ოჯახი, რომელიც დღეის მდგომარეობით წარმოადგენს Nidovirales რიგის ყველაზე დიდ ოჯახს, თავის მხრივ იყოფა ორ ქვეოჯახად: Letovirinae და Orthocoronavirinae [9-19].
Orthocoronavirinae ქვეოჯახი , რომელიც შეიცავს ადამიანის რამდენიმე პათოგენს, სეროლოგიური და გენეტიკური თვისებების მიხედვით შეიძლება დალაგდეს ოთხ ძირითად ქვეჯგუფად: ალფა-კორონავირუსი (Alphacoronavirus (α−CoV)), ბეტა-კორონავირუსი (Betacoronavirus (β−CoV)), გამა-კორონავირუსი (Gammacoronavirus (γ−CoV)) და დელტა-კორონავირუსი ( Deltacoronavirus– δ-CoV) [2,6,9,13]. ეს კლასიფიკაცია დაფუძნებულია მოლეკულაში ცილების თანმიმდევრობის განსხვავებაზე. β-CoV ჯგუფი შეიცავს ადამიანის კორონავირუსების – HCoVs-ების უმრავლესობას და თავის მხივ იყოფა ოთხ ხაზად – A , B, C და D [22,34].
ალფა და ბეტა კორონავირუსები აინფიცირეენ მხოლოდ ძუძუმწოვრებს. გამა და დელტა-კორონავირუსები კი – ფრინველებს, თუმცა ზოგიერთმა მათგანმა ასევე შეიძლება დააინფიციროს ძუძუმწოვრებიც. α- და β-CoV-ები ადამიანში იწვევს რესპირატორულ დაავადებებს, ხოლო ცხოველებში – გასტროენერიტულს [2-6].
ფილოგენეტიკურმა კვლევითმა მონაცემებმა აჩვენეს, რომ ღამურები და მღრღნელები არიან უმრავლესობა α-CoV და β-CoV ვირუსების ბუნებრივი მასპინძლები (რეზერვუარები), მაშინ როდესაც ფრინველები წარმოადგენენ γ -CoV და δ-CoV -ების ძირითად რეზერვუარებს [22].
2. ადამიანის კორონავირუსები
ათასწლეულების განმავლობაში კორონავირუსები მუდმივად ლახავდნენ სახეობრივ ბარიერებს და ამ უწყვეტი და ცვალებადი პროცესების შედეგად ზოგიერთი მათგანი გახდა მნიშვნელოვანი პათოგენი ადამიანებისთვის [14] .
დღეისათვის ცნობილია შვიდი სახეობის ადამიანის კორონავირუსი (HCoVs). მათ შორის HCoV-229E და HCoV-NL63 წარმოადგენენ α- CoV -ებს, დანარჩენი ხუთი : HCoV-OC43 [3], HCoV-HKU1, მძიმე მწვავე რესპირატორული სინდრომის კორონავირუსი – მმრს (SARS-CoV), ახლოაღმოსავლური რესპირატორული სინდრომის კორონავირუსი – MERS-CoV და SARS-CoV-2 განეკუთნება β-CoV-ების ხაზს. (იხ სურ.3) [14].
HCoV–229E, HCoV-OC43, HCoV-HKU1 და HCoV-NL63 კორონავირუსები იმუნოკომპონენტურ ადამიანებში, ჩვეულებრივ, იწვევენ მსუბუქ რესპირატორულ სიმპტომებს, როგორიცაა გაციება ან/და დიარეა[4]. მათგან განსხვავებით SARS-CoV, MERS-CoV და SARS-CoV-2 წარმოადგენს მაღალპათოგენურ კორონავირუსებს, რომლებიც იწვევენ სასუნთქი გზების მწვავე, მძიმე და პოტენციურად ფატალურ ინფექციას. კერძოდ, გარკვეული კატეგორიის პაციენტებში დიდია ალბათობა განვითარდეს მძიმე რესპირატორული დისტრეს-სინდრომი (ARDS) და ექსტრაპირულარული გამოვლინება [8,22-23],
შენიშვნა: ალფა და ბეტა კორონავირუსები შეიძლება მძიმე ფორმებში მიმდინარეობდეს შინაური საქონელშიც; ამ გვარის ვირუსებში შედგის ღორის ტრანსმისიური გასტროენტერიტის ვირუსი, ღორის ნაწლავური დიარეის ვირუსი (PEDV) და ახლო წარსულში გამოვლენილი ღორის მწვავე დიარეის კორონავირუსი (SADS-CoV) [6].
[3] 2008 წელს ICTV -მ ვირუსების ტაქსონომიის 2008.085-126V რედაქციაში HCoV-OC43 და სხვა მსგავსი სახეობების ვირუსები გააერთიანა ერთ სახეობად, რომელიც იწოდება Betacoronavirus 1.
[4]თუმცა ზოგიერთ მათგანს შეუძლია მძიმე ინფექციები გამოიწვიოს ჩვილ, მოზარდ და ხანდაზმულ ადამიანებში [12].
2.1 კორონავირუსების ფიზიკურ-ქიმიური თვისებები
კორონავირუსების ვირიონის შეფასებითი მოლეკულური მასა (Mr) შეადგენს 400×106. ვირონებს ახასიათებენ საქაროზაში ან ცეზიუმის ქლორიდში (CsCl) ცურვითი სიმკვრივით (ცურვადობით –buoyant density), რომელიც კორონავირუსის ნაწილაკებისთვის შეადგენს 1.15–1.20 გ სმ−3 და 1.23–1.24 გ სმ−3 შესაბამისად, ხოლო სედიმენტაციის – კოეფიციენტი (s20,w) ტოლია 300-დან 500 სვედბერგის (S) (Svedberg unit)) [2,24].
კორონავირუსები ავლენენ მაღალ მდგრადობას და სიცოცხლისუნარიანობას სხვადასხვა ტემპერატურისა და ტენიანობის პირობებში, ამასთან გამოირჩევიან დაშლის დაბალი სიჩქარით. ასე მაგალითად, 25 °C-ზე და 79% ფარდობითი ტენინანობის (Relative Humidity) პირობებში, აეროზოლაციიდან (ვირუსული ნაწილაკის გავრცელება აეროზოლის ფორმით) 60 წუთის შემდეგაც MERS-CoV-ი ინარჩუნებს დაინფიცირების უნარს. ოთახის ტემპერატურის პირობებში SARS-CoV-ს შეუძლია გაძლოს 1-5 დღე სისველეში, 10-19 დღე შარდში, 15 დღე სისხლში და 3 დღე ზედაპირზე [4-5]; ნაწილაკები მგრძნობიარეა სითბოსადმი (დიაპაზონი 56°C დან -75°C-მდე, სრული ინაქტივირებისთვის საჭირო დრო 60 წთ-იდან 45 წთ-მდე შესაბამისად) [24], ულტრაიისფერი, რენტგენული, გამა- და სხვა მაიონიზებელ დასხივებისადმი, ლიპიდურ გამხსნელების, ასევე არაიონურ სარეცხი საშუალებების, ფორმალდეჰიდისა და დამჟანგველებისადმი. შესაბამისად, კორონავირუსების გაუვნებელყოფა შესაძლებელია 75 % ეთანოლის, ეთერისა და ქლორისშემცველი სადეზინფექციო საშუალებების მეშვეობით [2-6, 24].
2.2 ადამიანის კორონავირუსების ქრონოლოგია – აღმოჩენიდან დღემდე
2002 წლამდე ცნობილი იყო, ადამიანის კორონავირუსის ორი სახეობა, რომელიც იმუნოკომპეტენტურ (ჯანმრთელ) ადამიანებში ძირითადად იწვევს მსუბუქ დაავადებას როგორიცაა გაციება. ისინი არ ითვლებოდა ადამიანებისთვის მაღალპათოგენურ ინფექციებად, მანამ, სანამ 2002 -2003 წწ-ში ჩინეთში, არ იფეთქა კორონავირუსით გამოწვეულმა მძიმე მწვავე რესპირატორულმა სინდრომა (Severe acute respiratory syndrome (SARS)), ხოლო მოგვიანებით (2012 წელს) ახლოაღმოსავლურმა რესპირატორულმა სინდრომა (Middle East respiratory syndrome MERS). SARS-CoV-მა, MERS-CoV-მა და ამჟამად მსოფლიოში მძვინვარე SARS-CoV-2-მა წარმოაჩინეს თუ რაოდენ დამანგრეველი და საშიში შეიძლება იყოს ადამიანის კორონავირუსული ინფექციები [12,22] .
2.2.1 HCoV-229 და HCoV-OC43 კორონავირუსები
1930-იანი წლების შუა პერიოდში ქათმის მძიმე რესპირატორული ინფექცია ითვლებოდა კორონავირუსებით გამოწვეულ პირველ იდენტიფიცირებულ დაავადებად. ეს ინფექცია შემდეგში ცნობილი იყო ფრინველების ინფექციური ბრონქიტის სახელწოდებით, რომელსაც იწვევს ფრინველის ინფექციური ბრონქიტის ვირუსი (infectious bronchitis virus (IBV), მოგვიანებით მას ოფიციალურად ეწოდა ფრინველის კორონავირუსი (Avian coronavirus) [8,15].
ადამიანის კორონავირუსი პირველად დაფიქსირდა 1965 წელს, როდესაც დევიდ ტირელიმა (D.Tyrrell) და მალკოლმ ბაინომ (Malcolm L. Bynoe), დიდ ბრიტანეთში, ყმაწვილი ბიჭის ცხვირის სეკრეტიდან გამოყვეს ახალი ვირუსი. ბავშვს ჰქონდა გაციების ტიპიური სიმპტომები, ამასთან შემჩნეულ იქნა, რომ ცხვირიდან აღებულ გამონაყოფს შეუძლია მათ მიერ დაგეგმილ კვლევაში ნებაყოფლობით ჩართული ჯანმრთელი ადამიანების დაინფიცირება ინტრანაზალური (ცხირშიდა) ინოკულაციის გზით (მოხალისეებში ვლინდებოდა გაციების სიმპტომები). ამ ვირუსს კვლევის ავტორებმა უწოდეს B814 (ამჟამად ცნობილია როგორც HCoV-229E-ის B814 შტამი). B814-ის კულტივირება შესაძლებელი იყო ადამიანის ტრაქეას ქსოვილებში, თუმცა არა უჯრედულ ხაზში, რომელიც იმ პერიოდში ფართოდ გამოიყენებოდა გაციების სხვა ცნობილი ეტიოლოგიური აგენტების გამოსაზრდელად [25-29].
იმავე პერიოდში დოროთი ჰამრემ (Dorothy Hamre) (ჩიკაგოს უნივერსიტეტიდან) და ჯონ პროქნოუმ (John Procknow) (მათი პუბლიკაციის მიხედვით კვლევა დაწყებულია 1962 წელს, ხოლო საკუთრივ პუბლიკაცია გამოქვეყნებულია 1966 წელს), გაციების სიმპტომების მქონე სტუდენტ-მედიკოსების სასუნთქი გზებიდან გამოყვეს და დაახასიათეს ხუთი ახალი ინფექციური აგენტი. ამ აგენტებიდან ერთ-ერთის – 229E შტამის გამოზრდა შესაძლებელი იყო WI-38 უჯრედებში [25,29]. იმავე პერიოდში დადგინდა, რომ ორივე – B814 და 229E ვირუსი მგრძნობიარე იყო ეთერის მიმართ და ინფიცირებისთვის საჭიროებდნენ ლიპიდშემცველ გარსებს [22,25].
პარალელურად მსგავსი სახის ვირუსების კვლევას ახორციელებდა მერილენდის ჯანდაცვის ნაციონალური ინსტიტუტების (National Institutes of Health (NIH) in Bethesda) მკვლევართა ჯგუფი კენ მაკინტოშის (Kenneth McIntosh) ხელძღვანელობით. ამ ჯგუფის მიერ გამოყოფილი ვირუსული შტამები აღნიშნულ იქნა OC (organ culture) აბრევიატურით (მაგ. HCoV-OC43 ), რამდენადაც მათი გამოზრდა მოხერხდა სასუნთქი გზების ორანულ კულტურაში. მეცნიერებმა იმთავითვე ყურადღება მიაქციეს იმ გარემოებას, რომ HCoV-OC43 და HCoV-229E-ით ინფექციით გამოწვეულ დაავადებას ჰქონდათ მსგავსი კლინიკური ნიშნები [22,25,32].
მოგვიანებით, ჯ.ალმეიდამ (June D. Almeida) და დ. ტირელმა (David. A. J. Tyrrell) აჩვენეს, რომ ზემოთ, ხსენებული ვირუსული ნაწილაკები მორფოლოგიურად იდენტური იყო ფრინველის ბრონქიტისა და თაგვის ჰეპატიტის ვირუსების. ვირუსულ ნაწილაკები იყო პლეომორფული და მათი ზომები ვარირებდა 80-150 ნმ-დე, გააჩნდათ მემბრანული გარსები მრავალრიცხოვანი წამახვილებული (ქიმისებრი) გამონაზარდებით [33]. ვირუსების ამ ჯგუფისთვის (229E, OC, B814, IBV , მათ შორის თაგვის ჰეპატიტის გამომწვევი ვირსუსი), 1968 წელს შემოღებულიქნა ტერმინი „კორონავირუსები“, რომელიც აღწერდა ამ ვირუსული აგენტების, ელექტრონული მიკროსკოპული გამოსახულებების მიხედვით საერთო მახასიათებელ მორფოლოგიას [29, 34-35]. მოგვიანებით, კერძოდ 1975 წელს „Coronaviridae“ ეწოდა ვირუსების ოჯახს, რომელშიც შედიოდნენ ზემოხსენებული ვირუსები [36-37].
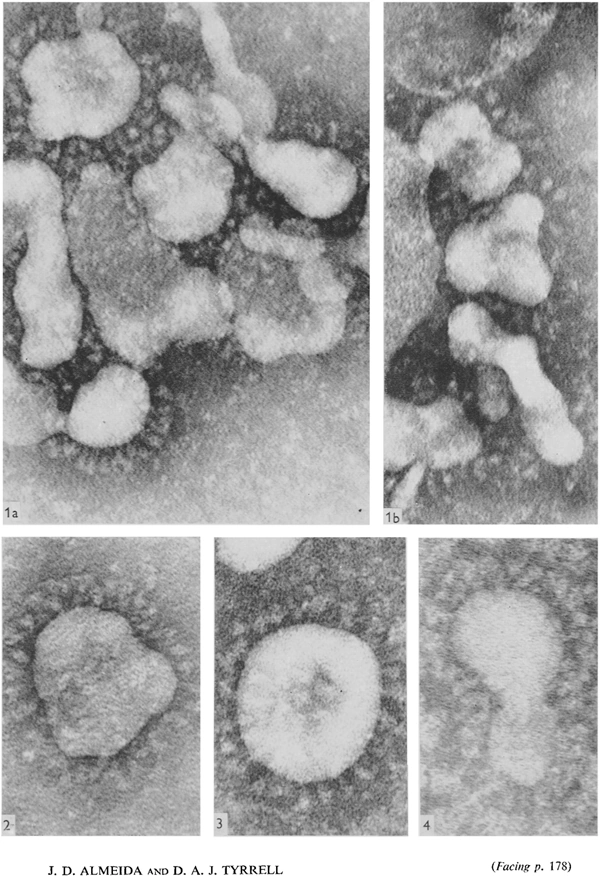
სურათი 4. ალმეიდას და ტირელის მიერ გადაღებული კორონავირუსების ტემ გამოსახულებები [33].
ამრიგად 2002 წლამდე ცნობილი იყო მხოლოდ ორი 229E და OC 43 ადამიანის კორონავირუსი, რომლებიც როგორც აღინიშნა ითვლება ნაკლებად პათოგენურად. კორონავირუსი HCoV-229E, ისევე როგორც HCoV-OC43 გავრცელებულია მთელს მსოფლიოში, მათ ახასიათებთ სეზონური ტენდენცია და უპირატესად თავს იჩენენ ზამთარში, ზომიერი კლიმატის პირობებში. 2002 წლამდე ადამიანებში გაციების სიმპტომების 15-30 % განპირობებული იყო სწორედ ამ ორი ვირუსით [42]. ორივე ვირუსის საინკუბაციო პერიოდი, როგორც წესი შეადგენს ერთ კვირაზე ნაკლებს, რასაც მოსდევს დაახლოებით 2-კვირიანი ავადმყოფობა. HCoV-229E-ით დაინციფირებულ ჯანმრთელ ადამიანებში ის მიმდინარეობს მსუბუქი გაციების სიმპომების სახით. დაქვეითებულ იმუნიტეტის მქონე პაციენტებში კი შესაძლოა გამოვლინდეს ქვედა სასუნთქი გზების მწვავე ინფექცია [22, 25].
2.2.2 მძიმე მწვავე რესპირატორული სინდრომის კორონავირუსი (SARS-CoV)
2002 წლის ნოემბერის შუა რიცხვებში, სამხრეთ ჩინეთში, კერძოდ კი გუანდუნის პროვინციის (Guangdong province) ფოშანის (Foshan) მუნიციპალიტეტში იფეთქა კორონავირუსით გამოწვეულმა მძიმე მწვავე რესპირატორული სინდრომა (SARS) [12,41-44].
მძიმე მწვავე რესპირატორული სინდრომის კორონავირუსი (SARS-CoV) (ასევე ცნობილი როგორც „ატიპური პნევმონია“), გახდა რიგით მესამე აღმოჩენილი ადამიანის კორონავირუსი – HCoV და ამასთან პირველი კარგად დოკუმენტირებული პანდემია კაცობრიობის ისტორიაში. მაღალპათოგენური ვირუსი სწრაფად გავრცელდა მსოფლიოს 30-ზე მეტ ქვეყანაში (გუანდინის პროვინციიდან ის გავრცელდა ჰონკონგში, შემდეგ ვიეტნამში, ჩრილოეთ ამერიკაში და ევროპაში) [22,41-42]. 2003 წლის ივლისის ბოლოსთვის დარეგისტრირდა 8098 ინფიცირებული, 774 გარდაცვალების ფაქტით (ლეტალობის მაჩვენებელი ≈ 9,5 % ) [12, 44-45].
ვირუსის საინკუბაციო პერიოდი შეადგენდა 4-7 დღემდე, ხოლო ვირუსული დატვირთვის პიკი დგებოდა ავადმყოფობის მე-10 დღეს . SARS-CoV-ით ინფიცირებულ პაციენტებს, თავდაპირველად აღენიშნებათ მიალგია (კუნთების ტკივილი), თავის ტკივილი, ცხელება, სისუსტე და შემცივნება, შემდეგ ქოშინი, ხოლო ხველა და სუნთქვის უკმარისობა გვიანდელი სიმპტომების სახით [41-42].
ლიმფოპენია, ღვიძლის ფუნქციის დარღვევა და მომატებული კრეატინკინაზას (ფერმენტი) მომატება წარმოადგენს SARS-ის ლაბორატორიულ გადახრებს. გართულებების შემთხვევაში პაციენტების 20-30 % საჭიროებს ინტენსიურ თერაპიას და მექანიკურ ვენტილაციას. ქვედა სასუნთქი გზების ტრაქტის გარდა, ინფექციამ შეიძლება გამოიწვიოს სხვა ორგანოების დაზიანებაც, მათ შორის კუჭ-ნაწლავის ტრაქტის, ღვიძლისა და თირკმელების. ასეთ მძიმე შემთხვევებს, ჩვეულებრივ, თან ახლავს ციტოკინური შტორმი, რაც შეიძლება აღმოჩნდეს ფატალური, განსაკუთრებით იმუნოკომპრომისულ (პატარა ბავშვებში და დაქვეითებული იმუნური სისტემის მქონე პირები) პაციენტებში [22, 41-42].
2.2.3 HCoV-NL63 და HCoV-HKU1
მას შემდეგ, რაც SARS-CoV ეპიდემიის ტალღამ გადაუარა კაცობრიობას და გამოვლინდა ამ სახეობის ვირუსების მაღალპათოგენურობა და სწრაფი გავრცელება, მსოფლიოს სხვადასხვა ქვეყნის წამყვანმა სამეცნიერო ჯგუფებმა უფრო მეტი ყურადღება გაამახვილეს კორონავირუსების კვლევებზე. დაიწყო ინტენსიური მუშაობა ახალი სახეობის კორონავირუსების აღმოჩენის კუთხით, რომელსაც შეეძლო ადამიანების, ასევე ღამურებისა და სხვა ცხოველების დაინფიცირება [42]. შედეგმაც არ დააყოვნა და მალევე აღმოჩენილ იქნა ადამიანის ორი ახალი კორონავირუსი HCoV-HKU1 და HCoV-NL63 [46-49].
მორიგი ახალი ადამიანის კორონავირუსი HCoV-HKU1 აღმოაჩინეს 2004 წლის იანვარში, მისი პირველი შტამი გამოყვეს 71 წლის მამაკაცისგან, რომელიც ჰონგ-კონგში პნევმონიითა და ბრონქიოლიტის სიმპტომებით გადმოყვანილ იქნა საავადმყოფოში [46]. ამის შემდეგ HCoV-HKU1– ვირუსი, მანამდე ცნობილი ადამიანის კორონავირუსების HCoV-229E და HCoV-OC43 მსგავსად გამოვლენილ იქნა მთელს მსოფლიოში. კორონავირუსის ეს ახალი სახეობა მმრს-სგან (SARS) განსხვავებით იწვევს მხოლოდ მსუბუქ რესპირატორულ ინფექციებს. HCoV-HKU1 ასოცირდება მწვავე ბრონქიოლიტთან, ასთმური გამწვავებით. ფებრილური გულყრის სიხშირე HCoV-HKU1-ით დაინფიცირებისას უფრო მაღალია, ვიდრე სხვა ადამიანის კორონავირუსული ინფექციისას [47]. შემთხვევათა უმრავლესობა ფიქსირდება ზამთარსა და გაზაფხულზე, როგორც წესი ის ემთხვევა გრიპის სეზონს [48].
2004 წლის ბოლოს, ჰოლანდიაში, 7 თვის ჩვილისგან, რომელსაც აღენიშნებოდა ბრონქიოლიტი და კონიუქტივიტი, გამოყვეს მომდევნო ახალი ტიპის კორონავირუსი HCoV-NL63 [49]. თავდაპირველად მიჩნეულ იქნა, რომ ის ვრცელდება მხოლოდ მცირეწლოვან ბავშვებში, ხანდაზმულებში, დაქვეითებული იმუნიტეტისა და რესპირატორული დაავადებების მქონე პაციენტებში [22]. HCoV-NL63-ით ინფიცირებისას ხშირად ვლინდება რინიტი (სურდო), კონიუნქტივიტი, ცხელება და ბრონქიოლიტი [50]. თავდაპირველად ჩაითვალა რომ ეს იყო ლოკალური ვირუსი, თუმცა შემდგომი კვლევებით გაირკვა, რომ იგი გავრცელებულია არა მარტო ჰოლანდიაში არამედ – მთელს მსოფლიოში [8]. ასევე დადგინდა, რომ HCoV-NL63 წარმოადგენს საერთო რესპირატორული დაავადებების დაახლოებით 4.7%-ს, ხოლო ინფექციის პიკურ შემთხვევებს ტროპიკულ და სუპტროპიკულ რაიონებში ადგილი აქვს ზაფხულის დასაწყისში და შემოდგომაზე, ხოლო ევროპის ქვეყნებში უმეტესწილად – ზამთარში [22,42].
2.2.5 SARS-2
2019 წლის ბოლოს, ჯანდაცვის მსოფლიო ორგანიზაციას ჩინეთის მთავრობამ მიაწოდა ინფორმაცია უცნობი ეტიოლოგიის მქონე პნევმონიის რამდენიმე შემთხვევის შესახებ. დაავადება პირველად დაფიქსირდა ჩინეთის პროვინცია ხუბეიში, კერძოდ კი ქალაქ უხანში. გავრცელების მთავარ ლოკაციად დასახელდა ხუანანის ზღვის პროდუქტების საბითუმო ბაზარი[5] (Huanan seafood market). დასაწყისში მსგავსი სიმპტომები გამოუვლინდა ორმოცდაათამდე ადამიანს [52].
[5] ხუანანის ცხოველებისა და ზღვის პროდუქტების საბითუმო ბაზარზე იყიდება ცოცხალი ცხოველები, როგორიცაა ღამურები, ბაყაყები, გველები, ფრინველები, ვირზაზუნები , კურდღლები და სხვ. [10].
2020 წლის 12 იანვარს, ჩინეთის ჯანდაცვის ეროვნულმა კომისიამ გაავრცელა დამატებითი ინფორმაცია ვირუსული ეპიდემიის შესახებ. ასევე დადგინდა, რომ დაავადების გამომწვევია ახალი კორონავირუსი. უფრო მეტიც, ვირუსული ინფექციის დიაგნოსტირებისათვის წარმოდგენილ იქნა გენეტიკური თანმიმდევრობა. თავდაპირველად გამოითქვა მოსაზრება, რომ პაციენტები, რომლებსაც დაუდგინდათ ამ ახალი კორონავირუსით გამოწვეული პნევმონია, შესაძლოა იყვნენ ზღვის პროდუქტების ბაზარში (სადაც იყიდება სხვადასხვა სახეობის ცხოველები და ქვეწარმავლები) და ჰქონდათ კონტაქტი ინფექციის მატარებელ ცხოველებთან ან შესაძლოა საკვებად იყენებდნენ დაავადებულ ცხოველებს ან/და ფრინველებს. ამასთან, შემდგომი გამოძიებით დადგინდა, რომ ზოგიერთი პირი ვირუსით დაინფიცირდა ისე, რომ შეხება არ ჰქონია ზემოაღნიშნულ ბაზართან. ამ დაკვირვებებმა აჩვენა, რომ ვირუსის გადაცემა შესაძლებელი იყო ადამიანიდან ადამიანზე. (ადამიანიდან ადამიანში ვირუსის გავრცელება ხდება ინფიცირებულ პირთან ახლო კონტაქით ხველებით, დაცემინებით, სუნთქვისას გამოყოფილი წვეთებით ან აეროზოლით) [52,57-58].
2019 წლის დეკემბრის შუა რიცხვებიდან დაწყებული, თვის ბოლომდე, პნევმონიის მქონე პაციენტების რიცხვმა საგრძნობლად იმატა. თავდაპირველად ახალი ვირუსი, ჩინელი მკვლევარების მიერ წოდებულ იქნა როგორც – უხანის კორონავირუსი (Wuhan coronavirus) [52], ხოლო ჯანმო-ს მიერ ვირუსი მოიხსენებოდა როგორც 2019 წლის ახალი კორონავირუსი (2019 novel coronavirus – 2019-nCov). მოგვიანებით, კერძოდ კი 2020 წლის თებერვალში ვირუსების ტაქსონომიის საერთაშორისო კომიტეტის (ICTV) მიერ მძიმე მწვავე რესპირატორული სინდრომის გამომწვევი აგენტი ოფიციალურად წოდებულიქნა როგორცβ-კორონავირუსი– 2 ანუSARS-CoV-2 (severe acute respiratory syndrome coronavirus 2) [52, 59].
2002 წლის SARS ვირუსით გამოწვეული დაავადებისგან განსხვავების მიზნით, ამჟამად, ჯანმო SARS-CoV-2-ით გამოწვეულ დაავადებას მოიხსენიებს როგორც კოროვირუსულ დაავადება 2019-ს (coronavirus disease 19 – COVID-19) [62].
განსაზღვრების მიხედვით კორონავირუსული დაავადება (COVID-19) წარმოადგენს ადვილად გადამდებ, პათოგენურ ვირუსულ ინფექციას. გენომურმა ანალიზმა აჩვენა, რომ SARS-CoV-2 ფილოგენეტიკურდ დაკავშირებულია მმრს-ებრ ღამურას ვირუსებთან, ამიტომაც შესაძლოა სწორედ ღამურები იყვნენ ვირუსის ძირითად რეზერვუარი. შუამავალი წყარო და ადამიანზე გადამცემის შესახებ ცალსახად დადასტურებული ინფორმაცია არ არის, თუმცა ადამიანიდან ადამიანზე სწრაფად გადაცემა ფართოდ დადასტურდა [7, 52-53].
SARS-CoV და MERS-CoV-ის მსგავსად, SARS-CoV-2-იც იწვევს რესპირატორულ ინფექციას, რომელიც ზოგიერთ პაციენტში იწვევს ვირუსულ პნევმონიასა და მწვავე რესპირატორული დისტრეს სინდრომს (ARDS). თუმცა, რესპირატორული სიმპტომების გარდა, SARS-CoV-2– ით უკონტროლო ინფექციამ შეიძლება გამოიწვიოს ციტოკინური შტორმი, რომლის დროსაც იმუნური სისტემა ანთების საწინააღმდეგო ციტოკინებსა და ქიმოკინებს წარმოქმნის ჭარბი რაოდენობით, რაც საბოლო ჯამში იწვევს სხვადასხვა ორგანოს დაზიანება [7]. გარდა ამისა, COVID-19 იწვევს კოაგულაციის დარღვევას პაციენტების მნიშვნელოვან ნაწილში, რამაც შეიძლება გამოიწვიოს თრომბოემბოლიური მოვლენები, ასევე განვითარდეს გულ-სისხლძარღვთა დაავადებები, როგორიცაა არითმია, მწვავე კორონარული სინდრომი (ACS) და სხვ.[60-61].
მანამდე ცნობილი ადამიანის კორონავირუსებისგან განხვავებით, ახალი კორონავირუსის ადვილი გადაცემის უნარის გამო, ინფექცია ძალიან სწრაფად გავრცელდა და მოკლე პერიოდში მოიცვა მთელი მსოფლიო, გამოიწვია რა კაცობრიობის არსებობის ისტორიაში ყველაზე ფართომასშტაბიანი პანდემია.
SARS-CoV-2-ი 2019 წლის დეკემბრიდან მოყოლებული დღემდე მძვინვარებს. ე. წ პირველი ტალღის (2019 წლის დეკემბრიდან -2020 წლის მაისი) მინელების შემდეგ, 2020 წლის სექტემბრის შუა რიცხვებიდან კვლავ დაიწყო გააქტიურება და მეორე ეპიდემიური ტალღის სახით კვლავ შემოუბრუნდა მსოფლიოს და საფრთხეს უქმნის გლობალურ საზოგადოებრივ ჯანმრთელობას.
მთელს მსოფლიოში, COVID-19 დადებითი შემთხვევების რიცხვი ყოველდღიურად ექსპონატურად იზრდება და ახლა დაჩქარებული ტემპებით ხორციელდება როგორც ეფექტური მკურნალობის გზების ძიება ისე და ახალი ვაქცინების და პრეპარატების შემუშავება.
3. ცხოველური წარმოშობა და კორონავირუსების ევოლუცია
3.1 ვირუსების ბუნებრივი მასპინძლები და შუამავალი გადამტანები
მანამ, სანამ ვირუსები ველური ბუნებიდან „გააკეთებდნენ ნახტომს“ და ინფიცირების გზით შეაღწევდნენ ადამიანის ორგანიზმში, ისინი განუწყვეტლივ ახორციელებდნენ თავიანთი გენომის მუტაციათა სერიებს [22].
მუტაცია და ადაპტაცია ასტიმულირებდნენ კორონავირუსების (CoV) და მათი მასპინძლების (მათ შორის ადამიანების) თანაევოლუციას მრავალი ათასწლეულის განმავლობაში [22,43].
ვირუსების უმრავლესობა ხშირად საჭიროებს შუალედურ მასპინძელს ვიდრე ის უშუალოდ დააინფიცირებს ადამიანს. ცხოველი-მასპინძლის გამოვლენას აქვს ძალზე დიდი მნიშვნელობა ადამიანის დაინფიცირების პროფილაქტიკაში. ცხოველებში CoV-მასპინძლის ურთიერთქმედებების შესწავლამ ასევე შეიძლება მოგვცეს მნიშვნელოვანი ინფრომაცია ადამიანებში CoV-ის პათოგენეზის შესახებ [22,43].
კორონავირუსების შესახებ ამომწურავი და მკაცრად დადასტურებული ცნობები ჯერ კიდევ არ არსებობს, ხოლო ბუნებაში მათი წარმოშობა კვლავ რჩება გამოცანად. მიუხედავად ამისა მეცნიერული კვლევების შედეგად დგინდება მათი პათოგენეზისა და ეპიდემიის საერთო კანონზომიერებები. სწორედ მეცნიერული კვლევის შედეგად დაგროვილი ცოდნის საფუძველზე კეთდება ცალკეული დასკვნები ამ ვირუსების წარმოშობის შესახებ [43].
უნდა აღინიშნოს, რომ პანდემიური ვირუსების გაჩენის ერთ-ერთ ძირითად მექანიზმს წარმოადგენს ვირუსების გენეტიკური მასალის რეკომბინაცია ან/და რეასორტაცია (Reassortment), როდესაც ხდება ერთი მასპინძელი უჯრედის ერთდროულად რამდენიმე ვირუსით დაინფიცირება. ამ დროს შესაძლებელია მივიღოთ სრულიად ახალი ვირუსული შტამი, რასაც ხშირად ადგილი აქვს კორონავირუსებში (სურ. 5).
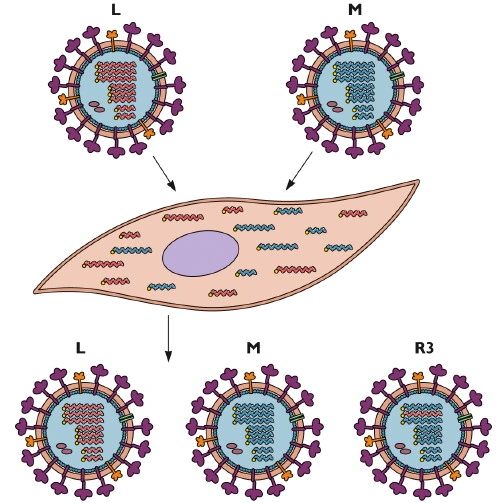
სურათი 5. ვირუსების რეასსორტაციის პროცესის სქემატური სურათი [64].
კორონავირუსების შემთხვევაში ყველაზე ხშირად რეკომბინაციული წყვეტები არის S გენის შემადგენლობაში, რომელიც შეიცავს S (spike) ცილას, ეს უკანასკნელი თავის მხრივ შეიცავს რეცეპტორ-მაკავშირებელ (ჩამჭერ) დომენს (RBD), რომელიც აკოდირებს დამატებით ცილას (რაზეც უფრო ვრცლად ქვემოთ ვისაუბრებთ).
ზემოთ ხსენებული გეთა რეასორტაცია წარმოადგენს რეკომბინაციის ერთ-ერთ სახეს და დამახასიათებელია სეგმენტირებული ვირუსებისთვის (კერძოდ, გრიპის ვირუსებისთვის). კორონავირუსებს გააჩნიათ არასეგმენტირებული რნმ, ამოტომაც მათვის შესაძლებელია რეკომბინაციის სხვა ვარიანტები, როდესაც ერთი სახეობის ვირუსს მეორე ვირუსში შეაქვს გენომის რაიმე ფრაგმენტი [53, 63].
ვირუსების ცვალებადობის მეორე მექანიზმი არის მუტაცია. რადგანაც დნმ-გან განსხვავებით, რნმ-ს რეპლიკაცია, ხორციელდება რეპარაციის (შეცდომების გასწორების) გარეშე, ამიტომაც რნმ-ს სინთეზისას შეცდომის დაშვების ალბათობა ათი ათასჯერ მაღალია, ვიდრე დნმ-ს რეპლიკაციისას. ყოველ რეპლიკაციურ ციკლში რნმ-ვირუსების დაახლოებით 10 % განიცდის მუტაციას. ეს შეიძლება იყოს ერთი ან რამდენიმე ნუკლეოტიდის ამოვარდნა ან პირიქით ჩამატება. რნმ-ს მუტაციები წარმოადგენს ანტიგენური დრეიფის – ანტიგენური მახასიათებლების ცვლილების ერთ-ერთ ძირითად წყაროს [53, 63].
სწორედ ზემოთხსენებული მექანიზმების გამო კორონავირუსები შედარებით ადვილად ახდენენ ახალ პირობებში ადაპტაციას და შესაბამისად დაპროგრამებულია შუამავალი მასპინძლების დიაპაზონის ეფექტურ მონაცვლეობაზე და ქსოვილების ტროპიზმზე. ამრიგად კორონავირუსებისგან მომდინარე საფრთხეები მუდივი და გრძელვადიანია. ზემოთქმულიდან გამომდინარე კორონავირუსების ვირუსოლოგიის საფუძვლიანი შესწავლა და მათი გავრცელების წინააღმდეგ ბრძოლას აქვს განსაკუთრებული მნიშვნელობა როგორც გლობალური ჯანმრთელობის ისე ეკონომიური სტაბილურობისთვის [6,64-65].
ვირუსების შესახებ დღეს არსებულ მონაცემთა ბაზებზე დაყრდნობით, ყველა ადამიანის კორონავირუს აქვს ცხოველური წარმომავლობა [12].
ვირუსების მასპინძელთა დიაპაზონის გაფართოების მიზეზს წარმოადგეს სხვადასხვა სახეობის ვირუსის მასპინძლებს შორის ფიზიკური კონტაქტი. ასევე ხელშემწყობი გარემოებაა კორონა ვირუსების მატარებელი სხვადასხვა სახეობების ცხოველების (ღამურების) განსახლების ტერიტორიების ახლო-ახლო (მეზობელი) მდებარეობა, რაც ხელს უწყობს ვირუსების სახეობათშორის, ჯვარედინი გადაცემის შესაძლებლობას. ასეთი შემთხვევების მაგალითს წარმოადგენს ჩინეთი, სადაც ღამურებს აქვთ ფართო გეოგრაფიული გავრცელება სახეობათა ფართო მრავალფეროვნებით (უნიკალური ქცევებით, დამახასიათებელი ფრენის სტილით, კვების რაციონით, ბინადრობა და მობილურობით) [8], რასაც ხელს უწყობს მათ საცხოვრისთან ახლოს სხვადასხვა წვრილფეხა და მსხვილფეხა მეცხოველეობის ფერმების მდებარეობა, რითაც იქმნება ხელშემწყობი პირობები ვირუსის მატარებელ ღამურებს, შუამავალ მასპინძელ ცხოველებს და ადამიანებს შორის მჭიდრო კონტაქტისთვის. (სურ. 6) [22,66].
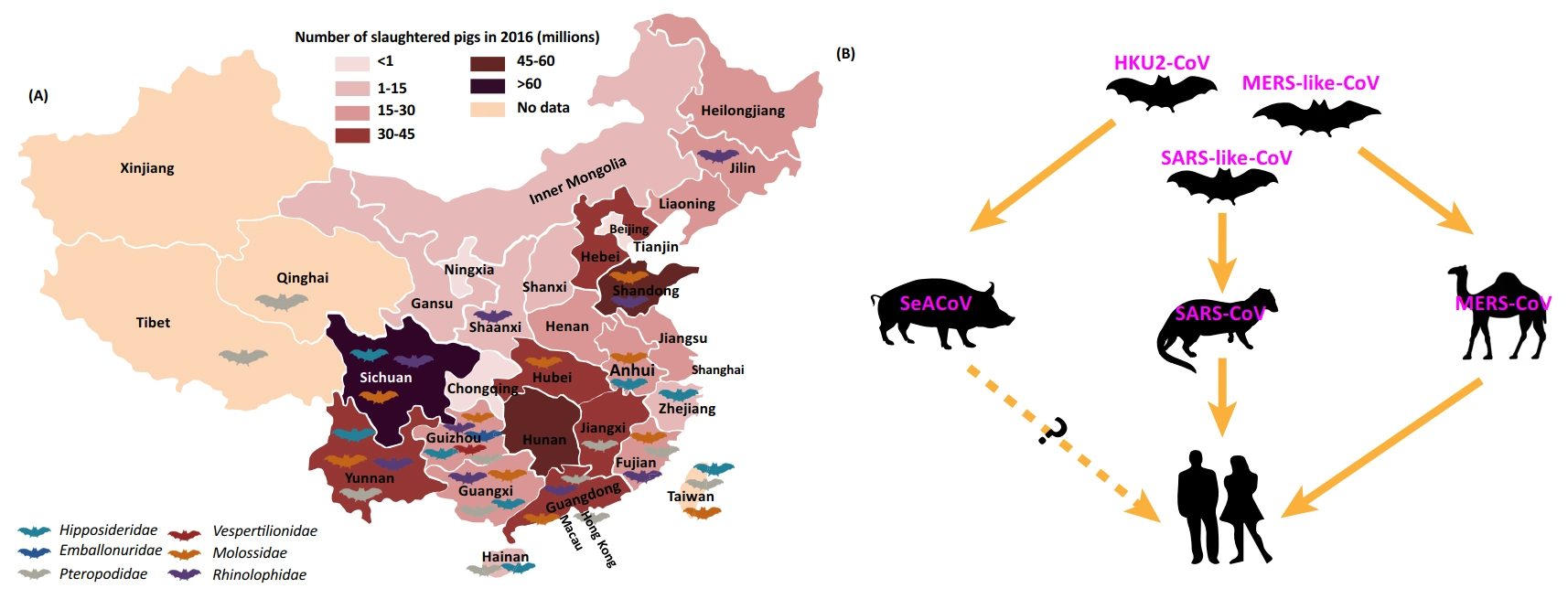
სურათი 6. ღამურების საცხოვრებელი არეალისა და ღორების ფერმების განლაგება (სიმჭიდროვის მიხედვით) ჩინეთის ტერიტორიაზე (A); ღამურის კორონავირუსების (HKU2-CoV) სახეობათშორისი გადაცემის სქემა (B) (პუნქტირული ხაზი მიუთითებს ვირუსის გადაცემის პოტენციურ, მაგრამ უცნობ გზას ღორიდან ადამიანზე [66].
ამრიგად მძიმე მწვავე რესპირატორული სინდრომის გამომწვევი კორონავირუსების გადამტანი ღამურების (SARSr-CoV – Severe acute respiratory syndrome–related coronavirus) ფართო გავრცელება და გენეტიკური მრავალფეროვნება, ასევე მათი მჭიდრო თანაცხოვრება და კორონავირუსების ხშირი რეკომბინაცია, მეცნიერთა ვარაუდით არის ვირუსების ახალი შტამების წარმოშობის საფუძველი. მეცნიერული კვლევებით მიღებულ შედეგებზე დაყრდნობით ივარაუდება, რომ SARS-CoV-ის პროგენიტორი (პირდაპირი წინაპარი) წარმოიქმნა ღამურებს შიგნით რეკომბინაციის გზით და შემდგომ გადაეცემა შუამავალ მასპინძლებს, ხოლო ამ უკანასკნელიდან ის შეიძლება გავრცელდეს ადამიანზე [12].
ქვემოთ ჩვენ უფრო დაწვრილებით განვიხილავთ დღეისათვის ცნობილი კორონავირუსების ძირითადი გადამტანი ცხოველები და მათი ადამიანზე გავრცელების გზებს.
3.2 HCoV-OC43 და HKU1-ის ბუნებრივი რეზერვუარი
ადამიანის ენდემური პათოგენი HCoV-OC43 წარმოადგენს BetaCoV1 სახეობის ვირუსის ერთ-ერთ შტოს. როგორც აღინიშნა, ის პირველად იზოლირებულიქნა 1960-იან წლებში. BetaCoV 1 განსხვავდება სხვა სახეობის კორონავირუსებისაგან იმით, რომ ის შეიცავს ისეთ შტამებს, რომლებიც გამოვლენილია ერთმანეთისგან ძლიერ განსხვავებულ მასპინძელ სახეობებში. მათგან ყველაზე კარგად შესწავლილია მსხვილფეხა რქოსანი პირუტყვის (BCoV–bovine CoV) ვირუსული შტამები, ამასთან, არსებითად იგივე ვირუსი გვხდება სხვა ჩლიქოსნებშიც (მაგ, ჟირაფებში, აქლემებში და სხვ). განსხვავებულ მასპინძელ ცხოველებში გამოვლენილი ყველა ეს ვირუსი განეკუთნება BetaCoV1– ვირუსებს. ბოლომდე ჯერ კიდევ არ არის გარკვეული თუ რატომ გვხდება BetaCoV1 შტამები ერთმანეთისგან რადიკალურად განსხვავებულ მასპინძელ სახეობებში. როგორც ჩანს სხვა CoV– ების მსგავსად, სახეობებს შორის რეკომბინაციამ და დელეციამ, ითამაშა განსაკუთრებული როლი ვირუსის მასპინძლებში ადაპტაციისა და გადაცემის პროცესებში [78,82-83].
ამრიგად ალფა და ბეტა კორონავისურსების სხვა სახეობებისგან განსხვავებით, BetaCoV1-ის, ასევე HCoV-HKU1 სახეობების ბუნებრივ მასპინძლებს (ბუნებრივ რეზერვუარებს – Natural reservoir) წარმოადგენენ არა ღამურები, არამედ მღრნელები [12,78,82-83].
3.3 HCoV-229E-ის ბუნებრივი მასპინძელი
ადამიანის რესპირატორული აგენტის HCoV-229E-ის პირველად აღმოჩენიდან (1962 წელი) 45 წლის შემდეგ, კერძოდ 2007 წელს, ამ ვირუსის გენომის მიმდევრობის მსგავსი მიმდევრობა აღმოჩენილი იქნა მოშინაურებულ ალპაკებში (Vicugna pacos) (ცხოველების ბაზრობაზე კალიფორნიაში). ცხოველებიდან აღებულ ვირუსულ შტამს ეწოდა ალპაკის კორონავირუსი (ACoV- Alpaca coronavirus ) და მოხერხდა მისი გენომის სრული სექვენირება. კვლევის შედეგებმა აჩვენა ძლიერი მსგავსება HCoV-229E-ის ცნობილ შტამების გენომის მიმდევრობასთან. საყურადღებოა ის ფაქტი, რომ ეს ვირუსული შტამი არ იქნა აღმოჩენილი ველურ (გარეულ) ინდივიდებში. ამ ფაქტის ასახსნელად ცალსახა პასუხის გაცემა აღმოჩნდა საკმაოდ რთული, რადგან ალბათობა იმისა, რომ მოშინაურებულ ცხოველებში ეპიდემიის მიზეზი ყოფილიყო ადამიანისაგან დაინფიცირება, იყო საკმაოდ დიდი. ამ უკანასკნელი მოსაზრების სასარგებლოდ მეტყველებდა ის ფაქტი, რომ დაახლოებით იმავე პერიოდში HCoV-229E– გენომის მსგავსი მიმდევრობის შტამები აღმოჩენილ იქნა აფრიკულ ღამურებში („hipposiderid“ ოჯახი) [71, 78-79] და გაკეთდა დასკვნები, რომ სწორედ ეს ღამურები წარმოადგენენ ამ სახეობის კორონავირუსის ბუნებრივ რეზერვუარს (რადგად ალპაკების განსახლების არეალს წარმოადგენს ამერიკის კონტინენტი, მათი დაინფიცირება ბუნებრივი მასპინძლებისგან შეუძლებელი იყო).
აღსანიშნავია, რომ სხვადასხვა კვლევითი ჯგუფების [84-85] მიერ 229Е-ს მსგავსი ვირუსული შტამები აღმოჩენილ იქნა ერთკუზიან აქლემებში (dromedary camels ) (აქვე შევნიშნოთ, რომ ალპაკა არის აქლემისებრი (Camelidae ) ოჯახის, ვიკუნია (Vicugna) გვარის ერთ-ერთი სახეობა).
ამრიგად არსებობს საფუძვლიანი ვარაუდი, რომ ვირუსის გადაცემა ადამიანზე შეიძლება მომხდარიყო აქლემებიდან ან სხვა უცნობი შუალედური მასპინძლიდან, ან/და უშუალოდ ღამურებიდანაც.
3.4 SARS-CoV-ის ბუნებრივი რეზერვუარი
2002 წელს SARS-CoV ეპიდემიის დასაწყისში, თითქმის ყველა ადრეული ინდექსის მქონე ინფიცირებულ პაციენტს დაავადების გამოვლენამდე ურთიერთობა ჰქონდა ცხოველებთან. SARS–ის გამომწვევი აგენტის დადგენის შემდეგ, SARS-CoV-ის საწინააღმდეგო ანტისხეულები აღმოჩენილ იქნა ჰიმალაიურ პალმის ცივეტებში (Paguma larvata) (ნიმუშები აღებულიქნა ცხოველთა ბაზრიდან) [12].
ზემოთქმულიდან გამომდინარე, ვირუსის ბუნებრივი რეზერვუარად თავდაპირველად მიჩნეულ იქნა პალმის ცივეტა (ციბეტა). მოგვიანებით, ფერმებსა და ველურ ბუნებაში ფართომასშტაბიანი კვლევის შედეგებზე დაყრდნობით გაკეთდა დასკვნები რომ, ცხოველების ბაზარში აღმოჩენილი SARS-CoV შტამები, ცხოველებს გადაედოთ სხვა ცხოველებიდან [12,43].
შემდგომი კვლევებით დადგინდა, რომ ადამიანის პირველი მაღალპათოგენური SARS-CoV-ის ბუნებრივ რეზერვუარს წარმოადგენს ცხვირნალისებრი ღამურები (Rhinolophus sinicus), რომლებსაც მეცნიერებმა მიაკვლიეს იუნანის პოვინციის ერთ-ერთ მღვრიმეში 2005 წელს [43]. მას შემდეგ რაც კვლევებით დადგინდა, რომ SARS-CoV- კორონავირუსის ბუნებრივ რეზერვუარს წარმოადგენს ღამურა, ცივეტა გახდა შუამავალი მასპინძელი [12].
გარდა პალმის ცივეტისა, მეცნიერებმა SARS-CoV-ი გამოავლინეს შინაურ კატაში, წითელ მელაში, ბატში, ბრინჯის ვირთხაში. ეს კორონავირუსი ასევე აღმოჩენილ იქნა ჩინეთში, გუანდუნის პროვინციის ცხოველთა ბაზრის მაჩვსა და ტახში [43].
ივარაუდება, რომ პალმის ცივეტას ვირუსი გადაედო იუნანის მღვრიმის ცხვირნამგალა ღამურებისგან, ხოლო ვირუსის მატარებელი ცივეტები შემდგომში გაიყიდა გუანდუნის ბაზარში, რამაც გამოიწვია ადამიანების დაინფიცირება SARS-CoV ვირუსით, რასაც მოჰყვა SARS-ის ინფექციის ეპიდემია [43,67].
3.5 MERS-CoV -ის ბუნებრივი რეზერვუარი
MERS-CoV-ის ძირითად ზოონოზურ წყაროდ (ბუნებრივ რეზერვუარად) თავდაპირველი კვლევებით მიიჩნეოდა ერთკუზიანი (არაბული) აქლემი (Camelus dromedaries) [68].
უფრო გვიანდელ კვლევებში MERS-კორონავირუსი ასევე აღმოჩენილ იქნა Perimyotis და Pipistrellus გვარის ღამურებში, რამაც გაზარდა ვარაუდი, რომ ვირუსების ძირითად რეზერვუარი არის სწორედ ღამურები [45,69-71].
სამეცნიერო ჯგუფის მიერ [80] ჩატარებული კვლევის მიხედვით, MERS-ვირუსის გენომის იდენტური მიმდევრობის მქონე შტამი აღმოჩენილ იქნა ეგვიპტურ – ე.წ სასაფლაოს ღამურის (Taphozous perforatus) ფეკალიებში [80-81].
ხაზგასასმელია ის ფაქტიც, რომ ზემოაღნიშნულ ღამურებში ინტრანაზალური და ინტრაპერიტონეალური გზებით MERS-ვირუსის ინოკულაცია იწვევს დაინფიცირებას, თუმცა არ ვლინდება დაავადების ნიშნები, რაც საკმაოდ დიდი ალბათობით მიუთითებს იმაზე, რომ სწორედ ღამურები წარმოადგენენ ვირუსის ბუნებრივ რეზერვუარებს, ხოლო ვირუსის შუალედურ მასპინძელს წარმოადგენს არაბული აქლემი (Camelus dromedaries) [69-71,81].
3.6. HCoV-NL63 -ის ბუნებრივი რეზერვუარი
როგორც ზემოთ ავღნიშნეთ HCoV-NL63 აღმოჩენილ იქნა 2004 წელს. ამერიკელი მკვლევარების მიერ იგივე ვირუსი RT-PCR მეთოდით იდენტიფიცირებულ იქნა 2005 წელს, რომელიც იწოდა როგორც HCoV-NH (ნაწარმოებია “New Haven coronavirus”-სგან) [77]. HCoV-NL63-თან დაკავშირებული ღამურის კორონავირუსები აღმოჩენილიქნა Vespertilionidae ოჯახის ევროპულ და აფრიკული ღამურებში [78]. თუმცა უფრო მოგვიანებით სხვა მკვლევარების მიერ წარმოდგენილი იქნა ღამურების Rhinonycteridae ოჯახის, Triaenops გვარის, Triaenops affer – აფრიკული სამკბილა ღამურების (African trident bat) სახეობის (კენია) ვირუსული შტამები, რომლებიც ავლენდნენ უფრო მჭიდრო კავშირს HCoV-NL63-თან. აღსანიშნავია, რომ ამ ღამურებს არ გააჩნიათ ახლო ნათესაობა წინამორბედი კვლევის Vespertilionidae ღამურებთან.
3.7 SARS-COV-2 -ის ბუნებრივი რეზერვუარი
დღეისათვის არსებული მონაცემებზე დაყრდობით, დიდი ალბათობით ივარაუდება, რომ SARS-COV-2-ის ბუნებრივ რეზერვუარს წარმოადგენს იუნანის პროვინციაში მიკვლეული ცხვირნალისებრი (Rhinolophus affinis) ღამურები. ვარაუდი ეფუძნება ვირუსის გენომის სექვენირების მონაცემებს[72-73].
აღმოჩნდა, რომ ერთ-ერთი პაციენტისგან აღებული SARS-CoV-2 ვირუსული შტამის გენომი 96%-იანი სიზუსტით იდენტურია ამ ღამურებში აღმოჩენილი Bat-CoV-RaTG13 [1] ვირუსული შტამის გენომის. მიუხედავად SARS-CoV-2 და Bat-CoV-RaTG13 შტამებს ზოგადი მსგავსებისა, ეს ორი ვირუსი განსხვავდება სპაიკ-ცილის მაკავშირებელი-რეცეპტორული დომენით (RBD) [72-73]. მიუხედავად გენების ასეთი ახლო მსგავსებისა არ შეიძლება გადაჭრით იმის თქმა, რომ სწორედ ეს ვირუსი წარმოადგენს SARS-CoV-2 კორონავირუსის რეკომბინაციის პირდაპირ შედეგს.
სწორედ ამის გამო SARS-COV-2-კორონავირუსის შემთხვევაშიც ივარაუდება, რომ არსებობს შუამავალი მასპინძლები. თავდაპირველ კვლევებში გამოითქვა ვარაუდი, რომ SARS-COV-2-ის შუამავალი მასპინძელი შესაძლოა იყოს გველი [74].
გარდა ამისა, მალაიზიიდან ჩინეთში შემოყვანილ პანგოლინებში (Manis javanica ) ასევე აღმოჩენილ იქნა კორონავირუსული შტამი, რომლის გენომს აქვს უფრო მაღალი იდენტური თანმიმდევრობა გენომის იმ კრიტიკულ სეგმენტთან, რომელიც პასუხისმგებელია მასპინძლის დაინფიცირებაში [73]. ამ კვლევებზე დაფუძნებით ივარაუდება, რომ SARS-COV-2 -ის შუამავალი მასპინძელი იყოს პანგოლინები [73, 75-76].
ჰომოლოგიური რეკომბინაციის შემდგომმა ანალიზმა აჩვენა, რომ ახალი კორონავირუსის მაკავშირებელი გლიკოპროტეინული სპაიკ რეცეპტორი ვითარდება SARS-CoV (CoVZXC21 ან CoVZC45) და ჯერ კიდევ უცნობი Beta-CoV ვირუსებიდან [70]. ვირუსის უფრო სრულყოფილად შესასწავლად საჭიროა მეტი სამუშაობეის ჩატარება შუალედური ზოონოზური წყაროს იდენტიფიცირების კუთხით, რომელმაც გამოიწვია ვირუსის გადაცემა ადამიანებში [23,52].
[1] ცნობილია რომ უშუალოდ Bat-CoV-RaTG13 შტამი არ იწვევს ადამიანების დაინფიცირებას.
ამრიგად, მძიმე მწვავე რესპირატორული სინდრომის გამომწვევი კორონავირუსების გადამტანი ღამურების SARSr-CoV (Severe acute respiratory syndrome–related coronavirus ) ფართო გავრცელება და გენეტიკური მრავალფეროვნება, ასევე მათი მჭიდრო თანაცხოვრება და კორონავირუსების ხშირი რეკომბინაცია, მეცნიერთა ვარაუდით არის ვირუსების ახალი შტამების წარმოშობის საფუძველი. მეცნიერული კვლევებით მიღებულ შედეგეზე დაყრდნიბით ივარაუდება, რომ SARS-CoV-ის პროგენიტორი (პირდაპირი წინაპარი) წარმოიქმნა ღამურებს შიგნით რეკომბინაციის გზით და შემდგომ გადაეცემა შუამავალ მასპინძლებს, ხოლო ამ უკანასკნელიდან ის შეიძლება გავრცელდეს ადამიანზე.
ზემო თქმულიდან გამომდინარე, ძალიან დიდი ალბათობით შეიძლება ითქვას, რომ ალფა- და ბეტა-კორონავირუსების ძირიდათ ბუნებრივ რეზერვუარს წარმოადგენს ღამურები [12].
ქვემოთ სურათ 7-ზე, მეტი თვალსაჩინოებისთვის წარმოდგენილია ყველა ზემოთ აღწერილი ადამიანის კორონავირუსების ბუნებრივი და შუამავალი მასპინძლები, მასპინძელ უჯრედებში ვირუსის სამიზნე რეცეპტორები, მათი აღმოჩენის თარიღები და ვირუსით გამოწვეული დაავადების სირთულე.
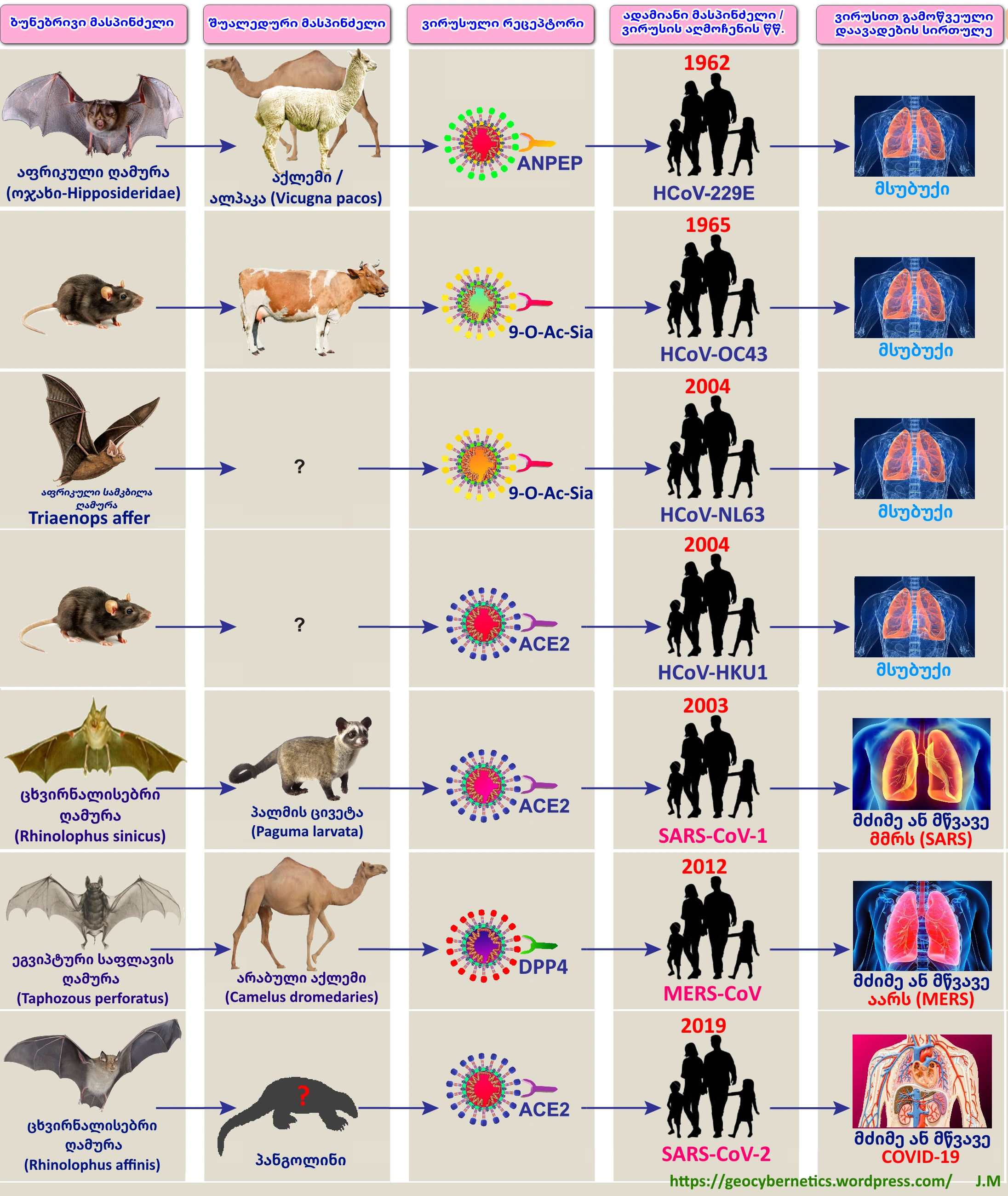
სურათი 7. ადამიანის კორონავირუსების ბუნებრივი და შუამავალი მასპინძლები, ქრონოლოგია და ვირუსით გამოწვეული დაავადების სირთულე. სხვადასხვა სახეობის ადამიანის კორონავირუსს შეიძლება გააჩნდეს სხვადასხვა ბუნებრივი და შუალედური მასპინძელი. ადამიანის კორონავირუსებიდან: HCoV-229E, HCoV-OC43, HCoV-NL63 და HCoV-HKU1 იწვევს მსუბუქ ინფექციას, მაშინ როდესაც SARS-CoV, MERS-CoV და SARS-CoV-2 შეიძლება მიმდინარეობდეს მსუბუქად ან პირიქით განვითარდეს მწვავედ და გამოიწვიოს ლეტალური შედეგიც; ადამიანის კორონავირუსები დასაინფიცირებლად (უჯრედში შესაღწევად) იყენებენ სხვადასხვა რეცეპტორებს კერძოდ : ANPEP-ს (ასევე ცნობილია როგორც CD13) – alanyl aminopeptidase, membrane (HCoV-229E) ; 9-0-Ac-Sia– 9-O-ს (9-O-acetylated sialic acids) -აცეტილირებული სიალური მჟავები (9-O-acetylated sialic acids) (HCoV-OC43, HCoV-NL63); ACE2 -ს ( angiotensin I-converting enzyme 2) – ანგიოტენზინ I-გარდამქნელი ფერმენტ 2 (აგფ 2) (HCoV-HKU1, SARS-CoV, SARS-CoV-2) და DPP4-ს (dipeptidyl peptidase 4 , ასევე ცნობილია როგორც CD26) – დიპეპტიდილ პეპტიდაზა 4 (MERS-CoV);
4. კორონავირუსების უჯრედში შეღწევის საკვანძო თავისებურებები და მექანიზმები
4.1 გენომის სტრუქტურა და საკვანძო ვირუსული ფაქტორები
SARS-CoV-2 კორონავირუსის აღმოჩენის მომენტიდან დაიწყო ამ ახალი ვირუსის გენომის მიმდევრობისა და ცილის სტრუქტურის ინტენსიური შესწავლა. დღეისათვის არსებული კვლევით მონაცემებზე დაყრდნობით ირკვევა, რომ SARS-CoV-2-სა და SARS-CoV-ს გააჩნიათ ძალიან ბევრი საერთო ბიოლოგიური მახასიათებლები, ასევე დადგინდა, რომ მათი გენური მიმდევრობის 79,6% იდენტურია [7, 76].
სხვა კორონავირუსების მსგავსად, SARS-CoV-2 -ის გენომი შეიცავს ათ ე.წ ღია წაკითხვის ჩარჩოს – ( ORFs – open reading frames), რომლებიც ახორციელებენ 24-დან 27-მდე გენის კოდირებას [7-8].
კორონავირუსების შემთხვევაში ORF– წარმოადგენს რნმ-ის შემადგენლობაში ნუკლეოტიდების თანმიმდევრობას, რომელსაც პოტენციურად შეუძლია ცილების კოდირება. ყველა კორონავირუსი შეიცავს სპეციფიკურ გენებს ORF1-ის ქვემოთ მდებარე უბნებში (არეებში), რომლებიც ახდენენ ვირუსის რეპლიკაციისთვის, ნუკლეოკაფსიდისა და ვირიონის გარე გარსზე არსებული გლიკოპროტეინული გამონაზარდების წარმოქმნისთვის საჭირო ცილების კოდირებას (სურ.8) [7-8, 52].
SARS-CoV-2-ის გენომის 5′ დაბოლოების ორი მესამედი, რომელიც ძირითადად განლაგებულია პირველ ORF-ში (ORF1a / ORF1b), ახორციელებს ორი პოლიპროტეინის (pp1a და pp1ab) ტრანსლირებას (კოდირებას), რომლებსაც ერთობლიობაში ეწოდება რეპლიკაზა. ეს პოლიპროტეინები იშლება (იხლიჩება) 1-16-მდე არასტრუქტურულ ცილად[1] (non-structural proteins–nps), მათ შორის რნმ- დამოკიდებულ რნმ პოლიმერაზად (RdRp – RNA-dependent RNA polymerase) და ორ ძირითად ვირუსულ პროტეაზად, სახელდობრ, 3-ქიმოტრიფსინის მსგავს პროტეაზად (3CLpro – 3-chymotrypsin like protease) და პაპაინის მსგავს პროტეაზად (PLpro – papain-like protease), ასევე ჰელიკაზად (Hel) და ექსონუკლეაზად (ExoN) (იხ.სურ 8) [7-8, 86].
SARS-CoV-2 გენომის 3 ′ -ის ერთ მესამედში, სხვა β-კორონავირუსების მსგავსად, ხორციელდება ოთხი ძირითადი სტრუქტურული ცილისა და რამდენიმე (ხუთიდან რვამდე) დამატებითი (დამხმარე) ცილის (accessory proteins) კოდირება [7-8, 52,86].
კორონავირუსების დამხმარე ცილები წარმოადგენენ ვირუს-სპეციფიკური ცილების ფართო ნაკრებს, რომლებიც ავლენენ შემოსაზღვრულ კონსერვაციას (ერთგვაროვნებას) ცალკეული სახეობების ფარგლებშიც კი. ითვლება, რომ მათ შეაქვთ წვლილი მასპინძელი უჯრედის ინფექციის მიმართ საპასუხო რეაქციის მოდულაციაში და წარმოადგენენ ვირუსული პათოგენურობის დეტერმინანტებს, ანუ სხვა სხვა სიტყვებით რომ ვთქვათ დამატებითი ცილები ეწინააღმდეგება მასპინძლის თანდაყოლილი იმუნური სისტემის საპასუხო რეაქციას [1]. აქვე უნდა აღინიშნოს, რომ უმრავლესობა დამატებითი ცილების მოლეკულური ფუნქციები არასაკმარისი ცოდნის გამო მნიშვნელოვანწილად კვლავ რჩება გაურკვეველი.
[1] ORF1a და ORF1b აკოდირებენ 15-16-მდე არასტრუქტურულ ცილას, რომელთაგან 15 შეადგენს ვირუსული რეპლიკაციისა და ტრანსკრიპციის კომპლექსს (RTC), რომელთა შორისაა რნმ-დამამუშავებელი, რნმ-მოდიფიცირებადი და რნმ-ფუნქციის შემმოწმებელი ფერმენტები, რომლებიც აუცილებელია კორონავირუსის გენის სრულყოფილად შენარჩუნებისთვის.
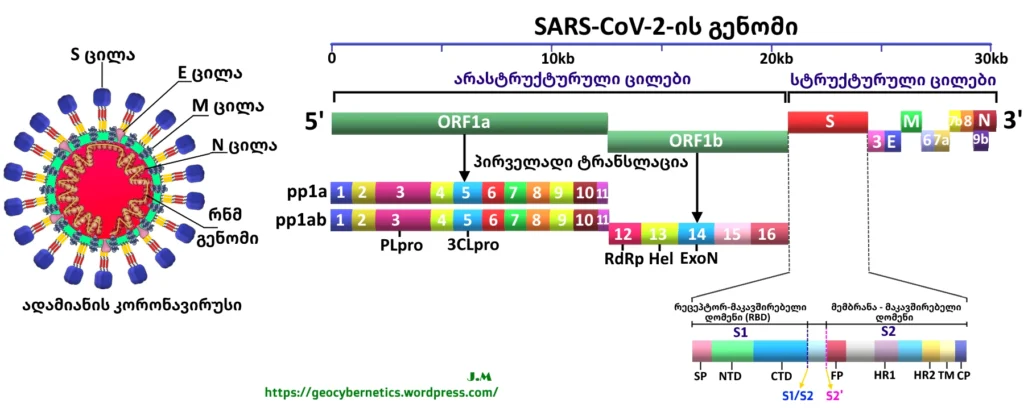
სურათი 8. კორონავირუსის ნაწილაკის (ვირიონის) და მისი გენომის სქემატური გამოსახულება. ა) ადამიანის კორონავირუსის სქემატური სურათი და ბ) მისი სრული გენომი. კორონავირუს გააჩნია ლიპიდური გარსი სამი სტრუქტურული ტრანსმემბრანული ცილით: ცილოვანი გამონაზარდი (S), მემბრანული ცილა (M) და გარსის ცილა (E). ვირუსის შიგნით მოთავსებულია ვირუსული გენომი, რომელიც ინკაფსულირებულია ნუკლეოკაფსიდური ცილით (N). CoV-ის ერთჯაჭვიანი გენომი ახორციელებს 16 არასტრუქტურული ცილის კოდირებას, მათ შორის პაპაინის მსგავს პროტეაზას (PLpro), 3-ქიმოტრიფსინის მსგავს პროტეაზად (3CLpro), რნმ-დამოკიდებულ რნმ-პოლიმერაზას (RdRp), ჰელიკაზას (Hel) და ექსონუკლეაზას (ExoN). სუბგენომური რნმ ახდენს ოთხი სტრუქტურული ცილის კოდირებას: სპაიკს (S; შინდისფერი), გარსის ცილას (E; მუქი ლურჯი), მემბრანულ ცილას (M; მწვანე) და ნუკლეოკაფსიდურ ცილას (N; ყავისფერი), ასევე სხვა დამხმარე ცილებს. კორონავირუსის S ცილა შედგება ორი სუბერთეულისგან: S1 და S2, რომლებიც მოიცავენ ძირითად ფუნქციონალურ კომპონენტებს: SP (სასიგნალო პეპტიდს), NTD (N-კიდურა დომენს), CTD (C-კიდურა დომენს), FP (ჰიბრიდულ პეპტიდს), HR1 (ჰეპტადურ გამეორება 1), HR2 (ჰეპტადური გამეორება 2), TM (ტრანსმემბრანული) და CP (ციტოპლაზამდური). S ცილას გააჩნია გახლეჩის ორი დომენი, რომელიც სურათზე აღნიშნულია ლურჯი (S1/S2) და ვარდისფერი (S2’) წყვეტილი ხაზებით.
როგორც აღინიშნა, კორონავირუსებში განსაკუთრებული როლს ასრულებს ოთხი ძირითდი სტრუქტურული ცილა – გლიკოპროტეინული გამონაზარდი – S, მცირე გარსის ცილა –E, მემბრანული ცილა – M და ნუკლეოკაფსიდს ცილა–N. SARS-CoV და SARS-CoV-2– ის შემთხვევაში ვირუსული S ცილის მიბმა სამიზნე რეცეპტორებთან იწვევს ვირუსის შეყვანას მასპინძელ უჯრედში, შესაბამისად S ცილისა და სამიზნე რეცეპტორებს (ACE2 ) შორის ურთიერთქმედების პროცესების შესწავლას აქვს განსაკუთრებული მნიშვნელობა ვაქცინის, ნეიტრალიზირებადი ანისხეულების ან ანტივირუსული ნაერთების შემუშავებისთვის.
კორონავირუსის S ცილები (ე.წ სპაიკები) წარმოადგენენ I კლასის ჰომოტრიმერულ შერწყმულ ტრანსმემბრანულ გლიკოპროტეინებს და არიან ვირუსის ყველაზე დიდ სტრუქტურები, მოლეკულური წონით ≈180–200 kDa (S ცილა ბოლოვდება N-ტერმინალით, რომელიც მოქცეულია არაუჯრედულ არეში და ვირუსულ მებრანასთანაა მიმაგრებული მისი ტრანსმემბრანული დომენით). ეს ცილები ძირითად როლს ასრულებენ მასპინძელ უჯრედის სპეციფიკურ რეცეპტორებთან შეკავშირებაში, უჯრედში შეღწევასა და დაავადების პათოგენეზში [ 7, 87].
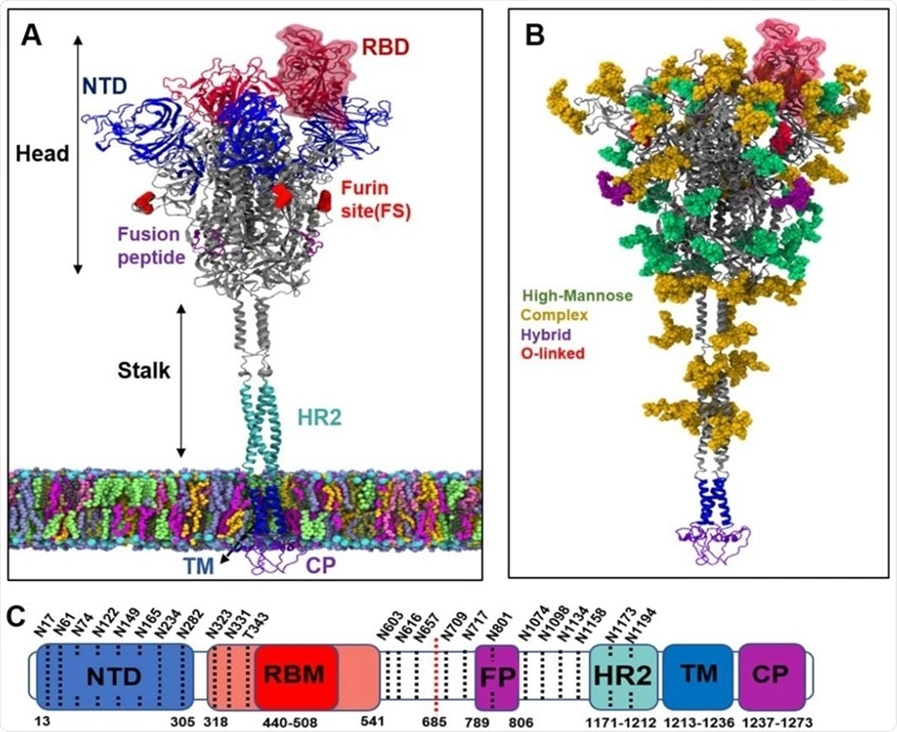
სურათი. 9 SARS-CoV-2-ის S ცილა (გლიკოპროტეინული გამონაზარდი) სხვა კორონავირუსების მსგავსად შედგება ორი ფუნქციურად განსხვავებული S1 და S2 სუბერთეულისგან (დომენისგან). S1 და S2 დომენი მასპინძელი უჯრედის დაიფიცირების პროცესში იხლიჩება. მათი ერთმანეთისგან განცალკევდება შეიძლება განხორციელდეს ან უშუალოდ მათი შეერთების ადგილას, ან ფერმენტ ფურინის (Furin) გაყოფის ადგილზე, TMPRSS2 (TMPRSS2 – transmembrane protease serine 2) პროტეაზას მეშვეობით, მას შემდეგ რაც ვირუსი შეკავშირედება მასპინძელი უჯრედის ACE2 რეცეპტორთან (იხ.სურ 8.) [8, 88].
S1 სუბერთეული შეიცავს ორ სუბდომენს, N-ტერმინალურ დომენს (NTD– N-terminal domain) და C-ტერმინალურ დომენს (CTD–C-terminal domain). ერთი ან ორივე სუბდომენი შეიძლება გამოყენებულ იქნას როგორც რეცეპტორ-მაკავშირებელი დომენი (RBD – receptor-binding domain), რომელიც პასუხისმგებელია ACE2-თან შეკავშირებაზე. RBD -ს გააჩნია რეცეპტორ-მაკავშირებელი მოტივი (RBM-receptor binding motif), რომელიც წარმოქმნის ჩაზენქილ ზედაპირს. ეს საშუალებას აძლევს მას ეფექტური კონტაქტი ჰქონდეს ACE2 მოლეკულის შესაბამის ამოზნექილ კიდესთან (იხ.სურ 8, სურ.9). არსებული ზოგადი წესის მიხედვით ითვლება, რომ NTD ხელს უწყობს ვირუსის შეკავშირებას ნახშირწყლების (საქარიდების) შემცველ რეცეპტორებთან, მაშინ როდესაც CTD ხელს უწყობს ცილის შემცველ რეცეპტორებთან შეკავშირებას, თუმცა არსებობს გამონაკლის შემთხვევებიც (მაგალითად თაგვის ჰეპატიტის ვირუსის NTD ამოიცნობს ცილოვან CEACAM1 რეცეპტორებს) [87-88].
ამრიგად, S1 ნაწილი საკვანძო ფუნქციურ დომენის – RBD-ის მეშვეობით განსაზღვრავს ვირუსისთვის მასპინძელთა სპექტრსა და უჯრედულ ტროპიზმს.
რაც შეეხება S2 სუბერთეულს – ტრანსმემბრანულ დომენს (TM ) (მას ასევე უწოდებენ შერწყმის სუბერთეულს), ის შეიცავს სხვადასხვა მოტივებს (სურ 8, სურ.9), მათ შორის შერწყმის პეპტიდს (FP–Fusion Peptide). FP აღწერს მოკლე სეგმენტს (15-25 ამინმჟავა), რომელიც კონსერვატულია ვირუსების მთელ ოჯახში, ის ძირითადად შედგება ჰიდროფობური ნაშთისგან, ისეთის როგორიცაა გლიცინი (G) და ალანინი (A), რომლებიც ჩაშენდებიან მასპინძელ-უჯრედში, რათა დაიწყოს შერწყმის პროცესი. შერწყმის პეპტიდები (FP), როგორც წესი მგრძნობიარეა წერტილოვანი მუტაციების მიმართ, რამდენადაც ერთ მუტაციას შეუძლია შეაჩეროს შერწყმა. ამრიგად S2 სუბერთეული უზრუნველყოფს ვირუსისა და მასპინძელი-უჯრედის მემბრანების შერწყმას ორი ტანდემური დომენის HR1 (heptad repeats 1) და HR2-ის მეშვეობით [ 7-8,31].
S ცილა ასევე მორთულია მრავალრიცხოვანი გლიკანებით, მათ შორის თითოეულ მონომერზე 22 N-გლიკანითა და 4 O-გლიკანით. უხეშად, რომ ვთქვათ გლიკანები ასრულებენ ფარის როლს და ეკრანირებას უკეთებენ ვირუსის სპაიკ ცილებს, რის გამოც ისინი შეუმჩნეველი ხდებიან იმუნური სისტემისთვის (ანტისხეულებისთვის). ამასთან, ასევე აღსანიშნავია, რომ SARS-CoV-2-ის S ცილა, SARS-CoV -ის S ცილისგან შედარებით ინარჩუნებს ადამიანის ACE2– რეცეპტორთან მიბმის უფრო მაღალ აფინურობას.
რაც შეეხება კორონავირუსების სხვა სტრუქტურულ ცილებს: გარსის მცირე (E) ცილები, რომლებიც გარსზე არსებობს მცირე რაოდენობით, როგორც ჩანს ძირითადად მოქმედებენ როგორც იონური არხები, რომელიც აუცილებელი არ არის ვირუსის რეპლიკაციისთვის, მაგრამ საჭიროა (აუცილებელია) პათოგენეზისთვის; მემბრანული/მატრიცული (M) ცილები ვირუსის სტრუქტურაში ყველაზე მეტად გავრცელებული ცილებია, რომლებიც პასუხიმგებელია ვირუსული მემბრანის გამრუდებაში და ნუკლეოკაფსიდთან მიერთებაში; ხოლო ნუკლეოკაფსიდური (N) ცილები – ახდენენ ვირუსული რნმ-ს გენომთან მიბმას და უზრუნველყოფენ რნმ-ს „ძაფზე ასხმული მძივები“-სებრ კონფიგურაციის შენარჩუნებას [89].
4.2 კორონავირუსის რეპლიკაცია და პათოგენეზი
კორონავირუსები ადამიანის უჯრედში შესასვლელად ძირითადი რეცეპტორების სახით უმეტესწილად იყენებენ („ამოიცნობენ“) ამინოპეპტიდაზებს ან ნახშირწყლებს, თუმცა მათგან განსხვავებით SARS-CoV და MERS-CoV ამოიცნობენ ეკზოპეპტიდაზებს. კორონავირუსის შეღწევის მექანიზმი დამოკიდებულია უჯრედულ პროტეაზებზე, რომლებიც შეიცავენ ადამიანის სასუნთქი გზების ტრიფსინის-მსგავს პროტეაზას (HAT–human airway trypsin-like protease), კატეფსინებსა (Cathepsins) და ტრანსმემბრანულ პროტეაზა სერინ 2 (TMPRSS2 – transmembrane protease serine 2) (იხ.სურ.10), რომლებიც ახდენენ „სპაიკ“ ცილების გახლეჩას და განსაზღვრავენ შეღწევის შემდგომ გზებს [52,86].
4.2.1 ვირუსის მიმაგრება და შეღწევა
კორონავირუსით დაინფიცირების საწყისი ეტაპი მოიცავს ვირუსის S ცილის სპეციფიკური მიბმას (შეკავშირებას) მასპინძელი უჯრედის რეცეპტორებთან, რომლებიც იდენტიფიცირებულია სხვადასხვა სახეობის კორონავირუსითვის, ეს რეცეპტორებია: ადამიანის ამინოპეპტიდაზა N (APN – aminopeptidase N) (ვირუსები – HCoV-229E, FeCoV, FIPV, TGEV და სხვ), დიპეპტიდილპეპტიდაზა 4 –DPP4 (dipeptidyl peptidase 4) (MERS-CoV) და ანგიოტენზინგარდამქმნელი ფერმენტ 2 (ACE2 – angiotensin-converting enzyme 2 ) (HCoV-NL63, SARS-CoV და SARS-CoV-2). აქვე უნდა აღინიშნოს, რომ არსებობს კორონავირუსების ისეთი სახეობები რომლებიც უჯრედში შესასვლელად არ იყენებენ ცილოვან რეცეპტორებს, ასე მაგალითად ხარის CV და ადამიანი HCoV-OC43 კორონავირუსები, სამიზნე უჯრედებში უკავშირდებიან სიალის მჟავის (sialic acid) ერთეულებს, რომელიც აღმოჩენილია გლიკოპროტეინებზე და გლიკოლიპიდებზე [10].
ამრიგად, უჯრედში შემყვანი რეცეპტორების ექსპრესია და ქსოვილური განაწილება ზეგავლენას ახდენს ვირუსულ ტროპიზმზე და პათოგენურობაზე [1,10].
4.2.2 კორონავირუსების ინფექციის ციკლი
სანამ უშუალოდ შეუდგებით რეპლიკაციის ციკლის დეტალურ განხილვას, მოკლედ განვიხილოთ ყველაზე უფრო მაღალპათოგენური კორონავირუსების (SARS-CoV, SARS-CoV-2, MERS) სამიზნე უჯრედებში შეღწევის ზოგადი სტრატეგიები.
როგორც ავღნიშნეთ კორონავირუსების S ცილა პასუხისმგებელია სამიზნე მასპინძელი-უჯრედების რეცეპტორებთან შეკავშირებასა და მის მემბრანასთან შერწყმაზე, შესაბამისად ეს პროცესი წარმოადგენს კრიტიკულ ეტაპს ვირუსის უჯრედში შესაღწევად (სწორედ ამიტომ, ვირიონის რეცეპტორთან შეკავშირების აფინურობის შესწავლას აქვს განსაკუთრებული მნიშვნელობა).
კვლევების შედეგად დადგინდა, რომ როგორც SARS-CoV-ი, ისე MERS-CoV ვირუსები ახდენენ პროტეაზების აქტივირებას. ასევე გაირკვა, რომ S ცილის სუბერთეულები (S1 / S2 და S2′) შესაძლებელია გაიხლიჩოს სხვადასხვა პროტეაზით. იმისათვის, რომ მოხდეს ვირუსისა და მასპინძელი უჯრედის მემბრანების შერწყმის რეაქციის კატალიზირება, S ცილა უნდა პრაიმირდეს შესაბამისი პროტეაზათი S1/S2 ინტერფეისზე და გააქტიურდეს (გააქტიურებული იქნას) უშუალოდ FP (S2 ′) ის გააქტიურებამდე (სურ 8-9). ამ პროცესში ყველაზე საყურადღებოა ის ფაქტი, რომ აქტივაცია შესაძლებელია განახორციელოს სხვადასხვა პროტეაზას მეშვეობით და აქედან გამომდინარე სწორედ პროტეაზები განსაზღვრავენ ვირუსულ ტროპიზმს. როგორც SARS-CoV, ისე MERS-CoV კორონავირუსების S ცილები უჯრედთან შესარწყმელად შეიძლება გააქტიურდეს ან პლაზმურ მებრანაზე, ან ენდოსომურ მემბრანაზე (Endosomal Membrane ), აქედან გამომდინარე ვირუსის უჯრედში შეღწევის გზები დამოკიდებულია შესაბამისი პროტეაზების ხელმისაწვდომობაზე (სურ.10) [90-91].
თუკი ვირიონისთვის ხელმისაწვდომია პლაზმური მემბრანის პროტეაზები, ვირუსს პლაზმურ მემბრანასთან შერწყმა შეუძლია ე.წ „ადრეული (მოკლე) გზით“ (“early pathway”), წინააღმდეგ შემთხვევაში ვირუსი უჯრედს შეერწყმება ენდოსომურ მემბრანაზე ე.წ „გვიანი (გრძელი) გზით“ (“late pathway”). აქ უნდა აღინიშნოს, რომ კორონავირუსის შერწყმის აქტივაცია დამოკიდებულია მოცემულ გარემოში პროტეაზის არსებობაზე (ნახ.3) [87,90-91].
თუ მემბრანა-მაკავშირებელი პროტეაზები (პირველ რიგში კი TMPRSS2 ) ხელმისაწვდომია მასპინძელ უჯრედში, მაშინ ვირუსული ნაწილაკის სამიზნე რეცეპტორთან „ადრეული შერწყმის“ გზით შეკავშირების შემდეგ, პროტეაზას (TMPRSS2-ს) შეუძლია გახლიჩოს ვირიონის S ცილები (გაწყვიტონ ცილის პეპტიდური ბმები) და შედეგად განხორციელდეს მასპინძელი უჯრედის პლაზმურ მემბრანასთან შერწყმა (იხ.ვიდეო 1, სურათი 10.) [87,90-91].
მაშასადამე, SARS-CoV-ები, ისევე როგორც MERS-CoV-ის ვირიონები, უჯრედის პლაზმურ მემბრანასთან შესარწყმელად მოითხოვს ბიოსინთეზის დროს S1 / S2 ინტერფეისის გახლეჩას. წინააღმდეგ შემთხვევაში ვირუსი დაექვემდებარება ენდოციტოზს – ამ დროს უჯრედის მაღალ მჟავა გარემოში ადგილი აქვს კატეფსინ L (cathepsin L)-ის გააქტიურებას, რასაც შეუძლია გამოიწვიოს შერწყმა ენდოსომურ მემბრანაზე (ენდოციტოზის დროს ვირიონი შემოსაზღვრულია უჯრედული მემბრანით და ინტერნალიზირდება ციტოპლაზმატური ვეზიკულების („ენდოსომების“) წარმოქმნის გზით (იხ სურ.10)) [87,90-91].
ამრიგად, უჯრედის ტიპისა და შესაბამისი პროტეაზების ხელმისაწვდომობის (არსებობის) მიხედვით, SARS-CoV, MERS-CoV და SARS-CoV-2 კორონავირუსებს მასპინძელ უჯრედში შეღწევა შეუძლია განახორციელონ ადრეული ან გვიანი გზების მეშვეობით [87]. ზოგადად ითვლება, რომ მაღალპათოგენური კორონავირუსები უჯრედში შესასვლელად პლაზმურ მემბრანასთან შერწყმის გზას (ე.წ „ადრეული გზა“) მიმართავენ ფილტვის უჯრედებში (რამდენადაც TMPRSS ჩვეულებრივ ექსპრესირდება ფილტვის უჯრედეში), ხოლო დანარჩენი ტიპის სამიზნე უჯრედებში ვირუსის შეღწევა ხორციელდება ენდოსომურ გზით.
ახალი კორონავირუსი SARS-CoV-2 -ს უჯრედში შესარწევად ასევე იყენებს ორივე გზას [87].
ამ მცირე გადახვევის შემდეგ კვლავ დაუბრუნდეთ კორონავირუსების რეპლიკაციის ძირითად ეტაპებს და განვიხილოთ ის უფრო დეტალურად.
4.2.3 კორონავირუსების რეპლიკაციის ციკლი
როგორც ზემოთ ავღნიშნეთ, SARS-CoV-ის ვირიონების მასპინძელ უჯრედში შეღწევის ორივე გზა ხორციელდება ძირითად რეცეპტორთან, კერძოდ კი ანგიოტენზინ-გარდამქნელი ფერმენტი 2 (ACE2 )-თან S-ცილის შეკავშირებით.
განვიხილოთ კორონავირუსების რეპლიკაციის ციკლი SARS-CoV-2-ის მაგალითზე.
რეპლიკაციის მთელი ციკლი მიმდინარეობს ციტოპლაზმაში და მოიცავს სრული (full-length) და სუბგენომური (sg) უარყოფით ჯაჭვიანი რნმ-ის შუალედური ნივთიერებების (intermediate) წარმოებას ( ვირუსულ გენომთან ერთად). ეს „ინტერმედიატები“ ასრულებენ როგორც ინფორმაციურლი-რნმ-ს (ი-რნმ) როლს (რეპლიკაზის პოლიპროტეინებისთვის), ისე მატრიცის როლს – უარყოფითი ჯაჭვის სასინთეზოდ [2, 8,89].
ინფექციის დროს – პირველ ეტაპზე, კორონავირუსის (ამ შემთხვევაში SARS-CoV-2 [1] ) S ცილები, ახორციელებენ შეკავშირებას (მიბმას) სამიზნე მასპინძელი უჯრედის ACE2 მემბრანულ რეცეპტორებთან. უფრო კონკრეტულად კი, S ცილა უჯრედგარეთა პროტეაზას (extracellular protease) მეშვეობით იყოფა ორ ფუნქციურ S1 და S2 სუბერთეულად (იხ. სურათი 10 (ეტაპი 1)). S1 სუბერთეულის RBD-ს მეშვეობით ACE2 რეცეპტორთან შეკავშირება, S2 სუბერთეულში იწვევს კონფორმაციულ ცვლილებას, კერძოდ ხორციელდება S2 სუბერთეულის გაყოფა და მისი აქტივირება მასპინძელი უჯრედის ზედაპირზე არსებული (თავმოყრილი) ტრანსმემბრანული პროტეაზა სერინ 2-ით (TMPRSS2) (იხ. სურ, ვიდეო 1-2). ყველა ეს მოქმედება იწვევს უჯრედის მემბრანისა და ვირუსის შერწყმას (როგორც ზემოთ ავღნიშნეთ ცალკეულ სამიზნე უჯრედებში შეიძლება ადგილი ჰქონდეს ენდოციტოზს). ეს მაღალაფინური ურთიერთქმედება აუცილებელია ვირუსის შეღწევისას, და შესაბამისად, წარმოადგენენ ძირითად სამიზნეებს COVID-19-ის მკურნალობისას.) (იხ.სურ. 10 ეტაპები 1a-1c)) [86, 89, 92-93].
მემბრანათა შერწყმის (ან ენდოსომის მეშვეობით ვირიონის უჯრედში შესვლის) შემდეგ, ვირუსული რნმ-გენომი გამონთავისუფლდება მასპინძელ-უჯრედის ციტოპლაზმში (იხ. სურ.10 ეტაპი 2) და ახლა უკვე უგარსო რნმ, ღია წაკითხვის ჩარჩოების – ORF1a და ORF1b-ის მეშვეობით ტრანსლირდება pp1a და pp1ab პოლიპროტეინებში შესაბამისად, რომლებიც შემდგომ, ვირუსის მიერ კოდირებული პროტეაზების – პაპაინ-მსგავსი პროტეაზის (PLpro) და 3C-მსგავსი პროტეაზის[2] (3CLpro-3) მეშეობით იშლება არასტრუქტურულ ცილებად (nsps) (სურ 10 ეტაპი 3-4). ეს ცილები (მათ შორის რნმ-დამოკიდებული რნმ-პოლიმერაზა – RdRp (RNA-dependent RNA polymerase), ჰელიკაზა – Hel (helicase), ექსონუკლეაზა – ExoN (exonuclease)) წარმოქმნიან რეპლიკაციურ-ტრანსკრიპციულ კომპლექსს – RTC-ს (replication-transcription complex)-ს და შეკავშირდებიან ორმემბრანულ ვეზიკულებთან (ბუშტუკებთან) – DMV (Double-Membrane Vesicles), რომლებიც წარმოიქმნება ენდოპლაზმური ბადისგან პრენუკლეარულ არეში, გარდა ამისა, ეს არე ასევე შეიცავს ხვეულ მემბრანებს – CM ( (convoluted membranes ) და მცირე ღია ორმაგი სფერული მემბრანებს – DMSs (small open double-membrane spherules). მთელი ეს სტუქტურა ქმნის დამცავ მიკროგარემოცვას, შემდეგ ეტაპზე ვირუსული გენომური რნმ-ს რეპლიკაციისა და სუბგენომური მ-რნმ-ს ( sg mRNAs) ტრანსკრიპციისთვის, რომელიც შეიცავს კორონავირუსის მახასიათებელ მ-რნმ ჩაშენებულ ნაკრებს (სურ 10, ეტაპი 5) [1, 8,87, 94-96].
ამრიგად RTC განუწყვეტლივ რეპლიცირებს და ასინთეზირებს სრულ უარყოფით (-) ჯაჭვიან რნმ-ს მატრიცას. ეს კომპლექსი მართავს (-) რნმ-ს წარმოქმნას რეპლიკაციისა და ტრანსკრიპციის მეშვეობით. რეპლიკაციის დროს წარმოიქნება (-) რნმ სრული ასლები, რომლებიც გამოიყენება მატრიცებად (+) რნმ გენომებისათვის. ტრანსკრიპციის დროს რნმ-ს შესაბამისი უბნები, მათ შორის ისინი რომლებიც ახდენენ ყველა სტრუქტურული ცილის კოდირებას, წარმოიქმნებიან წყვეტილი ტრანსკრიპციის მეშვეობით. ეს გზა გამოიყენება სრული რნმ გენომის რეპლიკაციისთვის და მათ შორის მ-რნმ-ის (mRNA) ინდივიდუალური სუბგენომური მატრიცების შესაქმნელად, რომელიც აუცილებელია ვირუსის სტრუქტურული და დამატებითი ცილების ტრანსლაციისთვის [89,94-95] (სურ 10, ეტაპი 6-7).
ტრანსლირებადი სტრუქტურული ცილები გადაადგილდებიან ენდოპლაზმური ბადის (ER) მემბრანებში და გადიან შუალედურ განყოფილებაში – ERGIC (ER-to-Golgi intermediate compartment), სადაც ხდება N-ინკაფსიდირება (სინთეზირებული სტრუქტურული და დამხმარე ცილები ასევე ტრანსპორტირდებიან ER-დან გოლჯის აპარატის მეშვეობით) (სურ 10, ეტაპი 8-9a). შემდეგ ეტაპზე ახლად წარმოქმნილი გენომური რნმ, ნუკლეოკაფსიდური ცილები და გლიკოპროტეინული გარსები იკრიბებიან და ქმნიან ვირუსული ნაწილაკების ჩანასახებს, რის შემდეგაც ახალი, ვირიონები გამოკვირტებიან გოლჯის ბუშტუკებში. საბოლოოდ, მომწიფებული SARS-CoV-2-ის ვირიონები ექვემდებარებიან ეკზოციტოზს და გამოთავისუფლდება მასპინძელის უჯრედიდან გარეთ, რათა გაიმეორონ ინფექციის ციკლი (სურ.10, ეტაპები 9-12) [1, 89, 95].
[1] SARS-CoV-2-ს გააჩნია კორონავირუსისთვის დამახასიათებელი ტიპიური სტრუქტურა, ის S ცილების გარდა (ცილოვანი გამონაზადების), ასევე ახდენს სხვა პოლიპროტეინების, ნუკლეოპროტეინების და მემბრანული ცილების, ისეთის როგორიცაა რნმ-პოლიმერაზა, 3-ქიმოტრიპსინის-მსგავსი პროტეაზა (3-chymotrypsin-like protease 3CLPro, პაპაინ-მსგავსი პროტეაზის (PLPro–papain-like protease), ჰელიკაზის (helicase), გლიკოპროტეინ და დამატებითი ცილების ექსპრესიას.
[2]კორინავირუსების გარდა 3CLpro ასევე წარმოადგენს მნიშვნელოვანი პროტეაზას მთელი რიგი ვირუსებისთვის, ისეთებისთვის როგორიცაა აივ და სხვ.
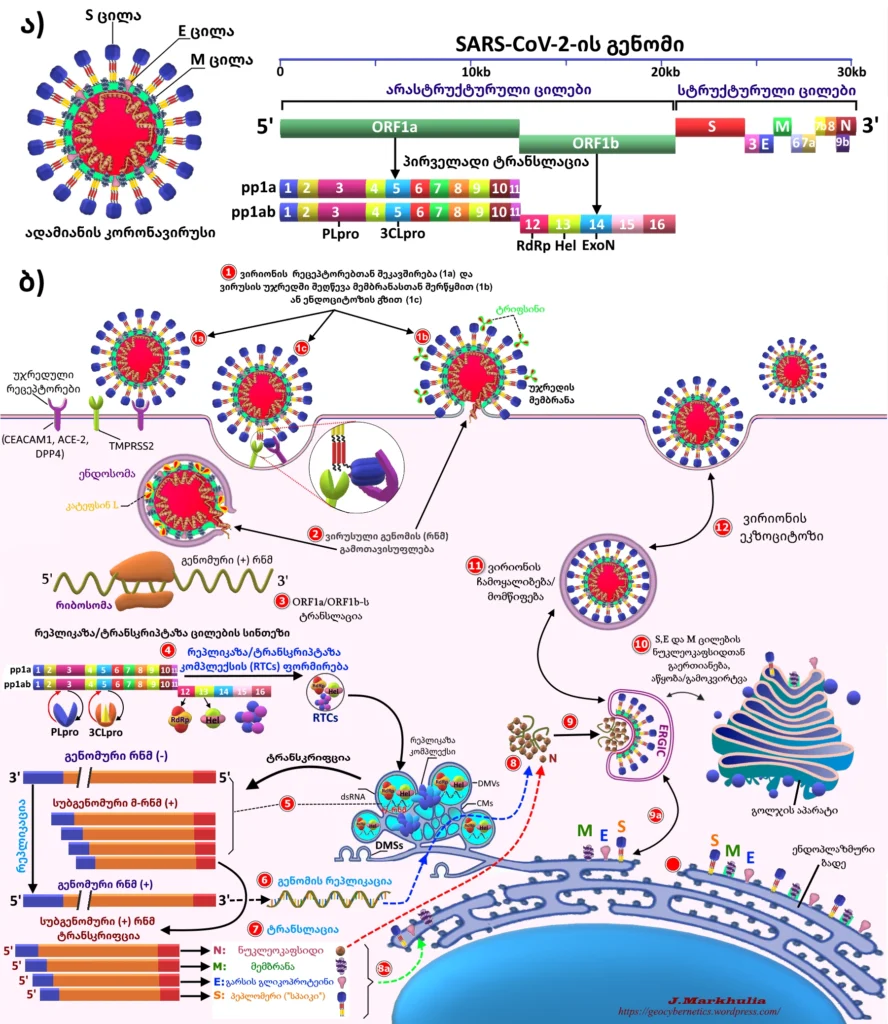
სურათი 10. SARS-CoV-2- ვირიონისა და გენომის სქემატური გამოსახულება (ა) და კორონავირუსის რეპლიკაციის ციკლის სქემატური მოდელი (ბ). კორონავირუსულ ნაწილაკს აქვს ცილებით შემოგარსული სფერული მორფოლოგია, რომელიც შედგება ოთხი სტუქტურული ცილისა და ერთჯაჭვიანი დადებითი (+) რნმ (ssRNA) გენომისგან სიგრძით ≈30 კბ. გენომის 5’ დაბოლოების 2/3-ი აკოდირებს pp1a და pp1ab პოლიპროტეინებს, რომლებიც იხლიჩება 16 სხვადასხვა არასტრუქტურულ ცილად. SARS-CoV-2 ით დაინფიცირება იწყება S ცილის სამიზნე მასპინძელი-უჯრედის ზედაპირზე არსებული ACE2 რეცეპტორთან შეკავშირებით (მიბმით) (ეტაპი 1). სქემატური მოდელი აღწერს ვირუსის მასპინძელ უჯრედში შეღწევის ორ გზას: ადრეულ და გვიანდელ გზას; რამდენადაც ვირიონი შეკავშირდება სამიზნე რეცეპტორთან (ეტაპი–1a), მას შეუძლია უჯრედში შეაღწიოს ან პლაზმური მემბრანასთან შერწყმის (ეტაპი 1b) ან ენდოსომის (ეტაპი 1c) მეშვეობით. SARS-CoV-ებისთვის ეგზოგენური ან მემბრანამაკავშირებელი პროტეაზების, ისეთების როგორიცაა ტრიფსინი და TMPRSS2, არსებობისას, შეღწევა ხორციელდება ადრეული შერწმის გზით, ანუ ვირუსილი კომპლექსი უჯრედის შიგნით ხვდება უჯრედულ მემბრანასთან პირდაპირი შერწყმითა და შემდგომ ციტოპლაზმაში გამოთავისუფლებით (ეტაპი 2), წინააღმდეგ შემთხვევაში ვირუსული ნაწილაკი უჯრედში აღწევს ენდოციტოზის მეშვეობით; ორივე შემთხვევაში ენდოსომის შიგნით დაბალი pH ახდენს კატეპსინ L- ის აქტივაციას, ხლეჩს რა „სპაიკ“ ცილის S2 სუბერთეულს, რთავს შერწყმის გზას და ციტოპლაზმაში გამოათავისუფლებს კორინავირუსის გენომს (ეტაპი 2). ციტოპლაზმაში გამოთავისუფლებული ვირუსული გენომის ღია წაკითხვის ჩარჩო (ORF1a/1b) ტრანსლირდება pp1a და pp1ab პოლიპროტეინებში (ეტაპი 3), რომლებიც შემდეგ იხლიჩება ვირუსული პროტეაზების მეშვეობით მცირე არასტრუქტურულ ცილებად, როგორიცაა რნმ-დამოკიდებული რნმ-პოლიმერაზა (RdRP) (ეტაპი 4). თავდაპირველად RTC მონაწილეობს (-) რნმ- სინთეზში, შემდგომში როგორც ერთჯაჭვიანი გენომური (+), ისე სუბგენომური რნმ-ს მისაღებად (ეტაპი 5). ვირუსული გენომური რნმ რეპლიცირდება RdRP -ს მეშვეობით (ეტაპი 6). სუბგენომური (+) რნმ-ს მეშვეობით ხორციელდება სტრუქტურული ცილების ტრანსლაცია (ეტაპი 7); ვირუსული ნუკლეოკაფსიდები იწყობა ახლადწარმოქმნილი გენომური რნმ-სა და N-ცილებისგან, რნმ-ს ნუკლეოკაფსიდის (N) ცილებში ინკაფსულირებით ციტოპლაზმაში (ეტაპი 8) და შემდეგ ხდება მისი ტრანსპორტირება (გადატანა) შუალედურ კომპარტმენრში ე.წ ERGIC-ში (ER–Golgi intermediate compartment)/გოლჯში შემდგომი აწყობისთვის (ეტაპი 9). გლიკოპროტეინული (S) , მემბრანული (M) და გარსული (E) ხვდებიან (ინერგებიან, გადადიან) ენდოპლაზმურ ბადეში ER (RER) (ეტაპი 8a), საიდანაც შემდგომ ხდება მათი ტრანსპორტირება ERGIC-ში (ეტაპი 9a), სადაც ხდება N-ცილებით ინკაფსულირებული რნმ-სთან ურთიერთქმედება და ვირუსული ნაწილაკის აწყობა (ეტაპი 10); ბოლოს, გენომური რნმ და სტრუქტურული ცილები თავს იყრიან ერთად და იწყობა ახალი ვირუსული ნაწილაკი (ეტაპი 11), ეს უკანასკნელი კი უჯრედიდან გამოთავისუფლდება ეკზოციტოზის მეშევეობით.
5. კორონავირუსებთან ბრძოლის სტრატეგიები
1.1 სპეციფიკური გამანეიტრალებელი ანტისხეულები
ვირუსის გამანეიტრალებელი ანტისხეულები, რომლებიც ინდუცირებულია ვაქცინებით ან ინფიცირებული ვირუსით, თამაშობს გადამწყვეტ როლს ვირუსულ ინფექციებთან ბრძოლაში.
თავდაპირველად პანდემიასთან საბრძოლველად შემუშავებული SARS-CoV და MERS-CoV კორონავირუსების გამანეიტრალებელი ანტისხეულები, ძირითადად შეიცავდა მონოკლონურ ანტისხეულებს –mAbs (monoclonal antibodies), მათ ფუნქციონალურ ანტიგენმაკავშირებელ ფრაგმენტს – Fab (functional antigen-binding fragment), ვარიაბელიური არის ერთჯაჭვიან ფრაგმენტს – scFv (single-chain variable region fragment), ან ერთდომენურ ანტისხეულებს – Nbs (single-domain antibodies (nanobodies) [86]. მათი სამიზნეები ძირითადად არის S1-RBD, S1-NTD ან S2 არე, ახდენენ რა RBD-ს შესაბამის რეცეპტორებთან (SARS-CoV შემთხვევაში ACE2, MERS-CoV-ის შემთხვევაში DPP4) შეკავშირების ბლოკირებას და ამით ხელს უშლიან S2 -ის შუამავლობით ვირიონისა და უჯრედის მემბრანების შერწყმას ან მასპინძელ უჯრედში შეღწევას, რითაც მცირდება დაინფეცირების ალბათობა [86,97]
ვირუსების გამანეიტრალებელი ანტისხეულების (ვგა) ძირითადი სამიზნეებისა და მოქმედების მექანიზმები, SARS- და MERS- კორონავირუსებისათვის ნაჩვენებია სურათ 11-ზე [86] . რაც შეეხება გამანეიტრალებელ მონოკლინურ ანტისხეულებს, მაგალითად ადამიანის mAbs-ები, როგორიცაა S230.15 და m396, მათი გამოყოფა მოხდა SARS-CoV-ით ინფიცირებული ადამიანებისგან. ისინი ახდენენ ადამიანისა და ცივეტის SARS-CoV -ინფექციას RBD-სთან ურთიერთქმედებით, რაც იწვევს ვირუსული RBD-ს უჯრედულ ACE2-თან შეკავშირების ბლოკირებას. საწყის პერიოდში ასევე მუშავდებოდა მსაგვსი მიდგომის სხვადასხვა SARS-CoV RBD-სპეციფიკური მანეიტრალებელი mAb (მაგალითად S109.8, S227.14, nAb 80R და სხვ) რომლებსაც გააჩნდათ საკმაოდ მაღალი ეფექტურობა უჯრედებზე ან ცხოველურ მოდელებზე ჩატარებული კვლევების მიხედვით, თუმცა ზემოთ ხსენებული არცერთი nAb SARS-CoV არ შეფასებულა კლინიკურ კვლევებით [1,86].
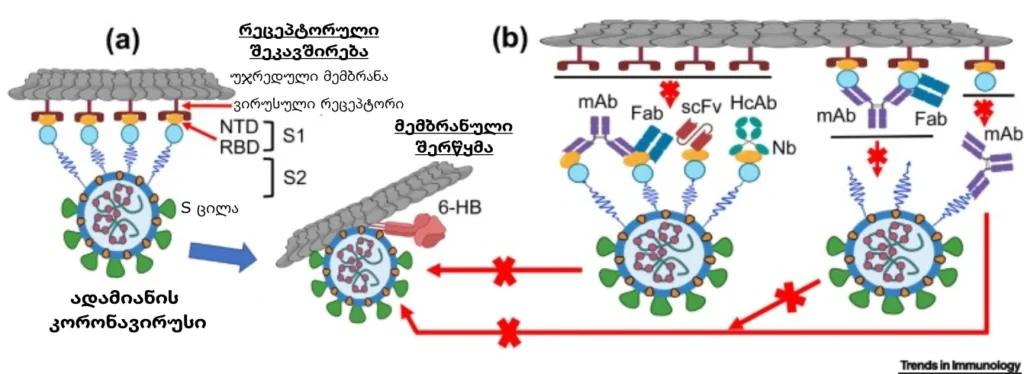
სურათი 11. კორონავირუსების საწინააღმდეგო სპეციფიკური გამანეიტრალებელი ანტისხეულების (nAbs) მოქმედების სქემატური წარმოდგენა. (a) ადამიანის CoV-ის რეცეპტორთან შეკავშირება და მემბრანათა შერწყმა. CoV თავდაპირველად ახდენს ვირუსის სამიზნე რეცეპტორების (ACE2 ან DPP4) შეკავშირებას (მიბმას) S-ცილის რეცეპტორ-მაკავშირებელი დომენის (RBD) მეშვეობით, რის შემდეგაც ხდება ვირუსის შერწყმა უჯრედულ მემბრანასთან ე.წ 6-HB-ის (six-helix bundle) ფორმირების გზით. (b) პოტენციური სამიზნეები (გამანეიტრალებელი ანტისხეულებისათვის (nAb)) ადამიანის კორონავირუსის S ცილაზე. მონოკლონური ანტისხეული (mAb), ანტიგენმაკავშირებელი ფრაგმენტი (Fab), ვარიაბელური არის ერთჯაჭვიანი ფრაგმენტი ((scFv) ან ერთდომენური ანტისხეული [ნანოსხეული ((Nb) ან VHH, რომელიც მიღებულია აქლემის ანტისხეულიდან (HcAb – camelid heavy chain antibody)] შეკავშირდება RBD-თან, ვირუსული S-ცილის S1 (რომელიც არ განეკუთნება RBD-ს, NTD-ს ჩათვლით) ან S2 სუბერთეული, რომელიც ახდენს RBD-სა და შესაბამისი რეცეპტორის შეკავშირების ბლოკირებას და ეწინააღმდეგება S-ცილის კონფორმაციულ ცვლილებას (S1-ზე მიმართული გამანეიტრალებელი ანტისხეულების შემთხვევაში ) ან ხელს უშლის S2-ით მეშვეობით მემბრანათა შერწყმას (S2-ზე მიმართული nAb-თვის), რაც საბოლოო ჯამში განაპირობებს უჯრედების CoV-ით დაინფეცირების ინჰიბირებას (დათრგუნვას)[86].
5.2 COVID-19-საწინააღმდეგო ვაქცინები და ვაქცინაცია
COVID-19-ის საწინააღმდეგო ვაქცინების შემუშავება, მათი მსოფლიოს სხადასხვა ქვეყნებში ოპერატიული განაწილება/მიწოდება და ვაქცინაციის მასშტაბური ჩატარება წარმოადგენს უმნიშვნელოვანეს ნაბიჯს არსებული პანდემიის ლიკვიდაციის, ჯანდაცვის სისტემის გამართული მუშაობისა და გლობალური ეკონომიკის აღდგენის გზაზე.
COVID-19 წარმოადგენს გლობალურ პრობლემას და შესაბამისად მასთან ბრძოლა უნდა ჰქონდეს საყოველთაო ხასიათი.
დღეისათვის არსებობს და უშუალოდ გამოყენებაშია COVID-19-ის საწინააღმდეგო რამდენიმე ვაქცინა. ჯანდაცვის მსოფლიო ორგანიზაციის (ჯანმო) ცნობით პირველი მასობრივი ვაქცინაციის პროგრამა დაიწყო 2020 წლის დეკემბრის დასაწყისში, ამ დღიდან მოყოლებული ვაქცინაციამ მიიღო ფართო ხასიათი და ის აქტიურად ხორციელდება მსოფლიოს მასშტაბით ბევრ ქვეყანაში. ამჟამად ძირითადად გამოიყენება სამი ტიპის 7 სხვადასხვა ვაქცინა [98].
ჯანმოს მიერ ნებადართული პირველი მ-რნმ ვაქცინა იყო Pfizer/BioNTech (BNT162b2) (2020 წლის 31 დეკემბერი). ხოლო 2021 წლის 15 თებერვალს ნებადართულ ვაქცინათა სიას დაემატა კომპანია AstraZeneca-სა და ოქსფორდის უნივერსიტეტის მიერ ერთობლივად შემუშავებული ვაქცინის ორი ვერსია, კერძოდ კი Serum Institute of India -სა და SKBio-ოს მიერ წარმოებული ვაქცინები (დამატებითი ცნობები Oxford/AstraZeneca ვაქცინის შესახებ ასევე შეგიძლია იხილოთ ჯანმოს საიტზე.
Moderna-ს COVID-19 საწინააღმდეგო ვაქცინა წარმოადგენს მატრიცულ რნმ (მ-რნმ) ვაქცინას. მასპინძელი-უჯრედები იღებენ ბრძანებას მ-რნმ-დან აწარმოონ S-ანტიგენის ცილები, რომელიც უნიკალურია SARS-CoV-2-თვის, რაც ორგანიზმს საშუალებას აძლევს მოახდინოს იმუნური პასუხის გენერირება და დაიმახსოვროს ეს ინფორმაცია იმუნური სისტემის მეხსიერების უჯრედებში [99]. ვაქცინა Moderna COVID ‑ 19 არ არის დამტკიცებული ან ლიცენზირებული აშშ-ს სურსათისა და წამლის ადმინისტრაციის (FDA) მიერ, თუმცა FDA-ს მიერ ის ნებადართულია გადაუდებელ შემთხვევებში გამოყენებისთვის [100]. მოდერნას ვაქცინის შესახებ უფრო მეტი ინფორმაციის ნახვა შეგიძლიათ ამ ბმულზე.
მოდერნას ვაქცინის მსგავსად აშშ-ს სურსათისა და წამლის ადმინისტრაციის (FDA) მიერ COVID ‑ 19-ის საწინააღმდეგოდ ექსტრემალური გამოყენებისთვის ნებადართულია Johnson & Johnson ვაქცინაც.
ქართულ ენაზე ვაქცინაციაზე და ვაქცინებზე მეტი ინფორმაციის ნახვა შეგიძლიათ აქ, ასევე ამ ბმულზე.
5.3 ვაქცინების ტიპები და მათი მოქმედების პრინციპები
სხვადასხვა ქვეყნის მეცნიერები დაუღალავად მუშაობენ COVID-19 -ის საწინააღმდეგო სხვადასხვა პოტენციური ვაქცინის შემუშავებაზე. ვაქცინის ძირითად ფუნქციას წარმოადგენს, ორგანიზმის იმუნურ სისტემას „ასწავლოს“ უსაფრთხოდ ამოიცნოს და გააუვნებელყოს/დაბლოკოს COVID-19-ის გამომწვევი ვირუსი.
ამჟამად შემუშავებულია სხვადასხვა ტიპის COVID-19-ის საწინააღმდეგო ვაქცინა მათ შორის:
- ინაქტივირებული ან დასუსტებული ვირუსული ვაქცინები, სადაც გამოიყენება ისეთი ინაქტივირებული ან დასუსტებული ვირუსი, რომელსაც არ შეუძლია ავადმყოფობის გამოწვევა, თუმცა ამასთან იწვევს იმუნური პასუხის გამომუშავებას (გენერირებას);
- ცილის საფუძველზე დამზადებული ვაქცინები, სადაც გამოიყენება ვირუსის ცილის უსაფრთხო ფრაგმენტები, რომლებიც ახდენენ COVID-19-ის იმიტაციას, რაც იწვევს ორგანიზმის იმუნური სისტემის თავდაცვითი პასუხის უსაფრთხო გენერირებას;
- ვექტორული ვირუსული ვაქცინები, რომლებიც შეიცავენ ადამიანისთვის უსაფრთხო ვირუს, რომელსაც არ ძალუძს ავადმყოფობის პროვოცირება, თუმცა გამოიყენება კორონავირუსული ცილების საწარმოებლად, რაც აუცილებელია იმუნური პასუხის ფორმირებისთვის;
- რნმ და დნმ–ვაქცინები. ეს არის ახლებური და მოწინავე მიდგომა ვაქცინების სფეროში, სადაც გამოიყენება გენეტიკურად მოდიფიცირებული რნმ ან დნმ რომლებიც ახორციელებენ უჯრედში ისეთი ცილების წარმოებას, რომლებიც შემდომში ხელს უწყობენ იმუნურ სისტემას უსაფრთხოდ გამოიმუშაოს იმუნური პასუხი დაავადების მიმართ [101].
რადგან ვაქცინები ახალი შემუშავებულია, ცალსახად იმის თქმა, ახდენენ თუ არა კოვიდის საწინააღმდეგო ვაქცინები მათ მიერ გამომუშავებული იმუნიტეტის ხანგრძლივი ვადით შენარჩუნებას ჯერ კიდევ ნაადრევია. ამ კითხვაზე დამაჯერებელი პასუხის გაცემა შესაძლებელი იქნება უფრო მეტი სამეცნიერო კვლევების ჩატარებისა და მიღებული ექსპერიმენტული მონაცემების ანალიზის შემდეგ.
იმედის მომცემია ის გარემოება, რომ არსებულ მონაცემებზე დაყრნობით COVID-19 გადატანილ პაციენტების უმრავლესობაში ფორმირდება იმუნური პასუხი (იმუნიტეტი), რომელიც გარკვეული პერიოდის განმავლობაში იცავს ხელმეორედ კორონავირუსით დაინფეცირებისგან, თუმცა თავდაცვის ინტენსივობა და ხანგრძლივობა ამ შემთხვევაშიც ცალსახად დადასტურებული არ არის და წარმოადგენს კვლევის საგანს.
გამოყენებული ლიტერატურა:
- V’kovski, P., Kratzel, A., Steiner, S. et al. Coronavirus biology and replication: implications for SARS-CoV-2. Nat Rev Microbiol (2020). https://doi.org/10.1038/s41579-020-00468-6
- Andrew M.Q. King, Chapter: Family Coronaviridae, Book: Virus Taxonomy, Elsevier, 2012, Pages 806-828, https://www.sciencedirect.com/science/article/pii/B9780123846846000689#s0175
- Pyankov OV, Bodnev SA, Pyankova OG, et al. Survival of aerosolized coronavirus in the ambient aid. J Aerosol Sci. 2018;115:158–163. doi:10.1016/j.jaerosci.2017.09.009
- Gan Y, Tan F, Yi R, Zhou X, Li C, Zhao X. Research Progress on Coronavirus Prevention and Control in Animal-Source Foods. J Multidiscip Healthc. 2020;13:743-751 https://doi.org/10.2147/JMDH.S265059
- Otter JA, Donskey C, Yezli S, et al. Transmission of SARS and MERS coronaviruses and influenza virus in healthcare settings: the possible role of dry surface contamination. J Hosp Infect. 2016;92:235–250. doi:10.1016/j.jhin.2015.08.027
- Li, F.Structure, Function, and Evolution of Coronavirus Spike Proteins Annual Review of Virology, 2016, 3, 237-261, https://www.annualreviews.org/doi/10.1146/annurev-virology-110615-042301
- Nishiga M, Wang DW, Han Y, Lewis DB, Wu JC. COVID-19 and cardiovascular disease: from basic mechanisms to clinical perspectives . Nat Rev Cardiol. 2020;1-16. doi:10.1038/s41569-020-0413-9
- Guo, Y., Cao, Q., Hong, Z. et al. The origin, transmission and clinical therapies on coronavirus disease 2019 (COVID-19) outbreak – an update on the status. Military Med Res 7, 11 (2020). https://doi.org/10.1186/s40779-020-00240-0
- Ashour, H.M.; Elkhatib, W.F.; Rahman, M.M.; Elshabrawy, H.A. Insights into the Recent 2019 Novel Coronavirus (SARS-CoV-2) in Light of Past Human Coronavirus Outbreaks. Pathogens 2020, 9, DOI: 10.3390/pathogens9030186
- Payne S. Family Coronaviridae. Viruses. 2017;149-158. doi: 10.1016/B978-0-12-803109-4.00017-9
- Lvov D.K., Alkhovsky S.V., Kolobukhina L.V., Burtseva E.I. Etiology of epidemic outbreaks COVID-19 in Wuhan, Hubei province, Chinese People Republic associated with 2019-nCoV (Nidovirales, Coronaviridae, Coronavirinae, Betacoronavirus, Subgenus Sarbecovirus): lessons of SARS-CoV outbreak. Problems of Virology, Russian journal. 2020;65(1):6-15. (In Russ.) https://doi.org/10.36233/0507-4088-2020-65-1-6-15
- Cui, J., Li, F. & Shi, Z. Origin and evolution of pathogenic coronaviruses. Nat Rev Microbiol 17, 181–192 (2019), https://doi.org/10.1038/s41579-018-0118-9
- Burrell CJ, Howard CR, Murphy FA. Coronaviruses. Fenner and White’s Medical Virology. 2017;437-446, doi: 10.1016/B978-0-12-375156-0.00031-X
- 14. https://fotospublicas.com/novo-sars-cov-2-de-coronavirus-micrografia-eletronica-de-transmissao-de-particulas-do-virus-sars-cov-2-isoladas-de-um-paciente/
- Kenneth J. Ryan et al. Sherris Medical Microbiology, Seventh Edition 7th Edition, ISBN: 978-1-25-985981-6, 2018 pp.181
- Fang Li, Structure, Function, and Evolution of Coronavirus Spike Proteins, J. Annual Review of Virology, Vol. 3:237-261, 2016, https://doi.org/10.1146/annurev-virology-110615-042301
- 17. https://talk.ictvonline.org/taxonomy/p/taxonomy_releases
- Cong Y, Verlhac P, Reggiori F. The Interaction between Nidovirales and Autophagy Components. Viruses. 2017;9(7):182. Published 2017 Jul 11. doi:10.3390/v9070182
- Rappe JCF, de Wilde A, Di H, et al. Antiviral activity of K22 against members of the order Nidovirales. Virus Res. 2018; 246:28-34. https://doi.org/10.1016/j.virusres.2018.01.002
- King, A. M.; Adams, M. J.; Carstens, E. B. & Lefkowitz, E. J. (Eds.) Order – Nidovirales Virus Taxonomy, Elsevier 2012, 784 – 794 , https://www.kau.edu.sa/Files/0011106/Subjects/Virus%20Taxonomy.pdf
- Kasmi Y, Khataby K, Souiri A, Ennaji MM. Coronaviridae: 100,000 Years of Emergence and Reemergence. Emerging and Reemerging Viral Pathogens. 2020;127-149. doi: 10.1016/B978-0-12-819400-3.00007-7
- Ye ZW, Yuan S, Yuen KS, Fung SY, Chan CP, Jin DY. Zoonotic origins of human coronaviruses. Int J Biol Sci 2020; 16(10):1686-1697. doi:10.7150/ijbs.45472. http://www.ijbs.com/v16p1686.htm
- Tang D, Comish P, Kang R (2020) The hallmarks of COVID-19 disease. PLoS Pathog 16(5): e1008536, https://doi.org/10.1371/journal.ppat.1008536
- Scheller, C., Krebs, F., Minkner, R., Astner, I., Gil‐Moles, M., & Wätzig, H. (2020). Physicochemical properties of SARS‐CoV‐2 for drug targeting, virus inactivation and attenuation, vaccine formulation and quality control. ELECTROPHORESIS. https://doi.org/10.1002/elps.202000121
- Jaiswal N.K., Saxena S.K. (2020) Classical Coronaviruses. In: Saxena S. (eds) Coronavirus Disease 2019 (COVID-19) pp 141-150. Medical Virology: From Pathogenesis to Disease Control. Springer, Singapore https://doi.org/10.1007/978-981-15-4814-7_12
- Mahase, E. (2020). Covid-19: First coronavirus was described in The BMJ in 1965. BMJ, m1547. https://doi.org/10.1136/bmj.m1547
- Tyrrell D.A.J, Bynoe M.L., Cultivation of a novel type of common-cold virus in organ cultures. Br med j. 1965;1(5448):1467-1470. https://doi.org/10.1136/bmj.1.5448.1467
- Steven h. Mylnt Human Coronavirus Infections CHAPTER 18, The Coronaviridae, edited by Stuart G. Siddell,Plenum Press, New York, 1995. https://doi.org/10.1007/978-1-4899-1531-3
- Tyrrell DA, Bynoe ML (1966) Cultivation of viruses from a high proportion of patients with colds. Lancet 1:76–77, https://doi.org/10.1016/S0140-6736(66)92364-6
- Hamre, D., & Procknow, J. J. (1966). A New Virus Isolated from the Human Respiratory Tract. Experimental Biology and Medicine, 121(1), 190–193. https://doi.org/10.3181/00379727-121-30734
- McIntosh K, Becker WB, Chanock RM (1967b) Growth in suckling-mouse brain of “IBV-like” viruses from patients with upper respiratory tract disease. Proc Natl Acad Sci U S A 58:2268–2273 https://doi.org/10.1073/pnas.58.6.2268
- Myint S.H. (1995) Human Coronavirus Infections. In: Siddell S.G. (eds) The Coronaviridae. The Viruses. Springer, Boston, MA. https://doi.org/10.1007/978-1-4899-1531-3_18
- June D. Almeida and D. A. J. Tyrrell The Morphology of Three Previously Uncharacterized Human Respiratory Viruses that Grow in Organ Culture, J. gen. Virol. (1967), 1, 175-178. https://doi.org/10.1099/0022-1317-1-2-175
- Yan, Y.; Shin, W.I.; Pang, Y.X.; Meng, Y.; Lai, J.; You, C.; Zhao, H.; Lester, E.; Wu, T.; Pang, C.H. The First 75 Days of Novel Coronavirus (SARS-CoV-2) Outbreak: Recent Advances, Prevention, and Treatment. Int. J. Environ. Res. Public Health 2020, 17, 2323. https://doi.org/10.3390/ijerph17072323
- Tyrrell, D. A. J., Almeida, J. D., Berry, D. M., Cunningham, C. H., Hamre D., Hofstad M. S., Mallucci L., McIntosh, K.: Coronaviruses. Nature (Lond.) 220, 650 (1968a). https://www.nature.com/articles/220650b0.pdf
- Tyrrell DA, Almeida JD, Cunningham CH et al (1975) Coronaviridae. Intervirology 5:76–82. https://doi.org/10.1159/000149883
- https://www.whatisbiotechnology.org/index.php/people/summary/Almeida
- Yasmin A. Malik, Properties of Coronavirus and SARS-CoV-2, Malaysian J Pathol 2020; 42(1) : 3 – 11, https://pubmed.ncbi.nlm.nih.gov/32342926/
- Abd El-Aziz TM, Stockand JD. Recent progress and challenges in drug development against COVID-19 coronavirus (SARS-CoV-2) – an update on the status. Infect Genet Evol. 2020;83:104327.https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7166307/
- 40. https://www.cdc.gov/coronavirus/types.html
- McIntosh K. Severe acute respiratory syndrome (SARS), UpToDate, Wolters Kluwer Health – 2012-05-09. http://www.uptodate.com/contents/severe-acute-respiratory-syndrome-sars
- To KK, Hung IF, Chan JF, Yuen KY. From SARS coronavirus to novel animal and human coronaviruses. J Thorac Dis. 2013;5 Suppl 2(Suppl 2):S103-S108. https://doi.org/10.3978/j.issn.2072-1439.2013.06.02
- Sun Z, Thilakavathy K, Kumar SS, He G, Liu SV. Potential Factors Influencing Repeated SARS Outbreaks in China. Int J Environ Res Public Health. 2020;17(5):1633. https://doi.org/10.3390/ijerph17051633
- ACE-2: The Receptor for SARS-CoV-2 .https://www.rndsystems.com/resources/articles/ace-2-sars-receptor-identified
- Wang, L.-F., & Eaton, B. T. (2007). Bats, Civets and the Emergence of SARS. Wildlife and Emerging Zoonotic Diseases: The Biology, Circumstances and Consequences of Cross-Species Transmission, 325–344. https://doi.org/10.1007/978-3-540-70962-6
- Woo PC, Lau SK, Chu CM, et al. Characterization and complete genome sequence of a novel coronavirus, coronavirus HKU1, from patients with pneumonia. J Virol. 2005;79(2):884-895. DOI: 10.1128/JVI.79.2.884-895.2005, https://jvi.asm.org/content/79/2/884
- Lau SK, Woo PC, Yip CC, et al. Coronavirus HKU1 and other coronavirus infections in Hong Kong. J Clin Microbiol 2006; 44:2063-71. https://doi.org/10.1128/JCM.02614-05
- Lee WJ, Chung YS, Yoon HS, et al. Prevalence and molecular epidemiology of human coronavirus HKU1 in patients with acute respiratory illness. J Med Virol 2013; 85: 309-14. https://doi.org/10.1002/jmv.23465
- Van der Hoek L, Pyrc K, Jebbink MF, et al. Identification of a new human coronavirus. Nat Med. 2004;10(4):368-373. https://doi.org/10.1038/nm1024
- Fouchier RA, Hartwig NG, Bestebroer TM, Niemeyer B, de Jong JC, Simon JH. et al. A previously undescribed coronavirus associated with respiratory disease in humans. Proc Natl Acad Sci U S A. 2004;101:6212-6. https://doi.org/10.1073/pnas.0400762101
- Skariyachan, S., Challapilli, S. B., Packirisamy, S., Kumargowda, S. T., & Sridhar, V. S. (2019). Recent Aspects on the Pathogenesis Mechanism, Animal Models and Novel Therapeutic Interventions for Middle East Respiratory Syndrome Coronavirus Infections. Frontiers in Microbiology, 10. https://doi.org/10.3389/fmicb.2019.00569
- Shereen, M. A.; Khan, S.; Kazmi, A.; Bashir, N. & Siddique, R. COVID-19 infection : Origin, transmission, and characteristics of human coronaviruses Journal of Advanced Research, 2020, 24, 91 – 98 . https://doi.org/10.1016/j.jare.2020.03.005
- Михаил Хецуриани. Великий комбинатор Как эволюционируют вирусы и каким станет SARS-CoV-2 . https://nplus1.ru/material/2020/03/18/virus-evolution
- Zhou, J., Chu, H., Li, C., Wong, B. H., Cheng, Z. S., Poon, V. K., et al. (2014). Active replication of Middle East respiratory syndrome coronavirus and aberrant induction of inflammatory cytokines and chemokines in human macrophages: implications for pathogenesis. J. Infect. Dis. 209, 1331–1342. https://doi.org/10.1093/infdis/jit504
- 55. https://www.who.int/csr/disease/coronavirus_infections/faq/en/
- Assiri, A., McGeer, A., Perl, T. M., Price, C. S., Al Rabeeah, A. A., Cummings, D. A., et al. (2013b). KSA MERS-CoV investigation team. hospital outbreak of middle east respiratory syndrome coronavirus. N. Engl. J. Med. 369:886. https://doi.org/10.1056/NEJMoa1306742
- L.T. Phan, T.V. Nguyen, Q.C. Luong, T.V. Nguyen, H.T. Nguyen, H.Q. Le, et al. Importation and human-to-human transmission of a novel coronavirus in Vietnam N Engl J Med (2020); https://doi.org/10.1056/NEJMc2001272
- Riou Julien, Althaus Christian L.. Pattern of early human-to-human transmission of Wuhan 2019 novel coronavirus (2019-nCoV), December 2019 to January 2020. Euro Surveill. 2020;25(4):pii=2000058. https://doi.org/10.2807/1560-7917.ES.2020.25.4.2000058
- World Health Organization. (2020). Novel Coronavirus (2019-nCoV): situation report, 10. World Health Organization. https://apps.who.int/iris/handle/10665/330775
- Connors JM, Levy JH. Thromboinflammation and the hypercoagulability of COVID-19. J Thromb Haemost. 2020 Jul;18(7):1559-1561. https://doi.org/10.1111/jth.14849
- Fan Y, Guo T, Lu Z. Myocardial Injury in COVID-19-Can We Successfully Target Inflammation?-Reply. JAMA Cardiol. 2020 Sep 1;5(9):1070-1071. DOI: 10.1001/jamacardio.2020.2572
- https://www.who.int/emergencies/diseases/novel-coronavirus-2019/technical-guidance/naming-the-coronavirus-disease-(covid-2019)-and-the-virus-that-causes-it
- https://www.worldometers.info/coronavirus/
- https://www.virology.ws/2009/06/29/reassortment-of-the-influenza-virus-genome/
- http://www.synthesis.cc/synthesis/2005/03/recombination_vs_reassortment#:~:text=The%20figure%20defines%20reassortment%20as,genome%2C%20potentially%20from%20the%20host
- Wang, L., Su, S., Bi, Y., Wong, G., & Gao, G. F. (2018). Bat-Origin Coronaviruses Expand Their Host Range to Pigs. Trends in Microbiology, 26(6), 466–470. https://doi.org/10.1016/j.tim.2018.03.001
- Chan PK, Chan MC. Tracing the SARS-coronavirus. J Thorac Dis. 2013;5 Suppl 2(Suppl 2):S118-S121. doi:10.3978/j.issn.2072-1439.2013.06.19
- Kulkarni D.D., Tosh C., Venkatesh G., Senthil Kumar D. Nipah virus infection: Current scenario. Indian. J. Virol. 2013;24:398–408. doi: 10.1007/s13337-013-0171-y.
- J. Huynh, S. Li, B. Yount, A. Smith, L. Sturges, J.C. Olsen, et al.Evidence supporting a zoonotic origin of human coronavirus strain NL63 J Virol, 86 (23) (2012), pp. 12816-12825; doi: 10.1128/JVI.00906-12
- J.F.-W. Chan, S. Yuan, K.-H. Kok, K.K.-W. To, H. Chu, J. Yang, et al.A familial cluster of pneumonia associated with the 2019 novel coronavirus indicating person-to-person transmission: a study of a family cluster Lancet (2020). https://doi.org/10.1016/S0140-6736(20)30154-9
- Corman VM, Muth D, Niemeyer D, Drosten C. Hosts and Sources of Endemic Human Coronaviruses. Adv Virus Res. 2018;100:163-188. DOI: 10.1016/bs.aivir.2018.01.001
- Zhou, P., Yang, XL., Wang, XG. et al. A pneumonia outbreak associated with a new coronavirus of probable bat origin. Nature579, 270–273 (2020). https://doi.org/10.1038/s41586-020-2012-7
- Matthew C. Wong, Sara J. Javornik Cregeen, Nadim J. Ajami, Joseph F. Petrosino , Evidence of recombination in coronaviruses implicating pangolin origins of nCoV-2019. doi: https://doi.org/10.1101/2020.02.07.939207
- Ji W., Wang W., Zhao X., Zai J., Li X. Homologous recombination within the spike glycoprotein of the newly identified coronavirus may boost cross-species transmission from snake to human. J. Med. Virol. :2020. DOI: 10.1002/jmv.25682
- Liu P., Chen W., Chen J.-P. Viral Metagenomics Revealed Sendai Virus and Coronavirus Infection of Malayan Pangolins (Manis javanica) Viruses. 2019;11:979. DOI: 10.3390/v11110979
- Wu F., Zhao S., Yu B., Chen Y.-M., Wang W., Song Z.-G., Hu Y., Tao Z.-W., Tian J.-H., Pei Y.-Y., et al. A new coronavirus associated with human respiratory disease in China. Nature. https://doi.org/10.1038/s41586-020-2008-3
- Esper F, Weibel C, Ferguson D, Landry ML, Kahn JS. Evidence of a novel human coronavirus that is associated with respiratory tract disease in infants and young children. J Infect Dis. 2005;191(4):492-498. doi: 10.1086/428138
- Corman V.M., Baldwin H.J., Tateno A.F., Zerbinati R.M., Annan A., Owusu M., Nkrumah E.E., Maganga G.D., Oppong S., Adu-Sarkodie Y., Vallo P., da Silva Filho L.V., Leroy E.M., Thiel V., van der Hoek L., Poon L.L., Tschapka M., Drosten C., Drexler J.F. Evidence for an ancestral association of human coronavirus 229E with bats. J. Virol. 2015; 89:11858–11870. DOI: 10.1128/JVI.01755-15
- Pfefferle S., Oppong S., Drexler J.F., Gloza-Rausch F., Ipsen A., Seebens A., Muller M.A., Annan A., Vallo P., Adu-Sarkodie Y., Kruppa T.F., Drosten C. Distant relatives of severe acute respiratory syndrome coronavirus and close relatives of human coronavirus 229E in bats, Ghana. Emerg. Infect. Dis. 2009;15:1377–1384.
- Memish ZA, Mishra N, Olival KJ, Fagbo SF, Kapoor V, Epstein JH, et al. Middle East Respiratory Syndrome Coronavirus in Bats, Saudi Arabia. Emerg Infect Dis. 2013;19(11):1819-1823. https://dx.doi.org/10.3201/eid1911.131172
- Mohd, H.A., Al-Tawfiq, J.A. & Memish, Z.A. Middle East Respiratory Syndrome Coronavirus (MERS-CoV) origin and animal reservoir. Virol J13, 87 (2016). https://doi.org/10.1186/s12985-016-0544-0
- Hu B., Zeng L.P., Yang X.L., Ge X.Y., Zhang W., Li B., Xie J.Z., Shen X.R., Zhang Y.Z., Wang N., Luo D.S., Zheng X.S., Wang M.N., Daszak P., Wang L.F., Cui J., Shi Z.L. Discovery of a rich gene pool of bat SARS-related coronaviruses provides new insights into the origin of SARS coronavirus. PLoS Pathog. 2017;13(11) e1006698
- Mittal A, Manjunath K, Ranjan RK, Kaushik S, Kumar S, Verma V (2020) COVID-19 pandemic: Insights into structure, function, and hACE2 receptor recognition by SARS-CoV-2. PLoS Pathog 16(8): https://doi.org/10.1371/journal.ppat.1008762
- Corman V.M., Eckerle I., Memish Z.A., Liljander A.M., Dijkman R., Jonsdottir H., Juma Ngeiywa K.J., Kamau E.,Younan M., Al Masri M., Assiri A., Gluecks I., Musa B.E., Meyer B., Muller M.A., Hilali M., Bornstein S., Wernery U., Thiel V., Jores J., Drexler J.F., Drosten C. Link of a ubiquitous human coronavirus to dromedary camels. Proc. Natl. Acad. Sci. U. S. A. 2016;113:9864–9869. https://doi.org/10.1073/pnas.1604472113
- Sabir JS, Lam TT, Ahmed MM, Li L, Shen Y, Abo-Aba SE, Qureshi MI, Abu-Zeid M, Zhang Y, Khiyami MA, Alharbi NS, Hajrah NH, Sabir MJ, Mutwakil MH, Kabli SA, Alsulaimany FA, Obaid AY, Zhou B, Smith DK, Holmes EC, Zhu H, Guan Y. Co-circulation of three camel coronavirus species and recombination of MERS-CoVs in Saudi Arabia. Science. 2016 Jan 1;351(6268):81-4. Epub 2015 Dec 17. PMID: 26678874. DOI: 10.1126/science.aac8608
- Jiang S., Hillyer C. Du L., Neutralizing Antibodies against SARS-CoV-2 and Other Human Coronaviruses,J. Trends in Immunology VOLUME 41, ISSUE 6, P545, JUNE 01, 2020, DOI: https://doi.org/10.1016/j.it.2020.04.008
- Tang, T., Bidon, M., Jaimes, J. A., Whittaker, G. R., & Daniel, S. (2020). Coronavirus membrane fusion mechanism offers as a potential target for antiviral development. Antiviral Research, 104792. DOI: 10.1016/j.antiviral.2020.104792
- Mahdi Ghorbani, Bernard R. Brooks, Jeffery B. Klauda, Exploring dynamics and network analysis of spike glycoprotein of SARS-COV-2, bioRxiv 2020.09.28.317206; doi: https://doi.org/10.1101/2020.09.28.317206
- Spotlight on COVID-19: Infection https://www.invivogen.com/spotlight-covid-19-infection
- Liu, J., Cao, R., Xu, M. et al. Hydroxychloroquine, a less toxic derivative of chloroquine, is effective in inhibiting SARS-CoV-2 infection in vitro. Cell Discov 6, 16 (2020). https://doi.org/10.1038/s41421-020-0156-0
- Zhou D, Dai SM, Tong Q. COVID-19: a recommendation to examine the effect of hydroxychloroquine in preventing infection and progression. J Antimicrob Chemother. 2020;75(7):1667-1670. doi: 10.1093/jac/dkaa114
- Hoffmann, M. et al. SARS-CoV-2 Cell Entry Depends on ACE2 and TMPRSS2 and Is Blocked by a Clinically Proven Protease Inhibitor. Cell. 2020 https://doi.org/10.1016/j.cell.2020.02.052
- Yamamoto, M. et al. 2016. Identification of Nafamostat as a Potent Inhibitor of Middle East Respiratory Syndrome Coronavirus S Protein-Mediated Membrane Fusion Using the Split-Protein-Based Cell-Cell Fusion Assay. Antimicrob Agents Chemother 60, 6532-6539. doi: 10.1128/AAC.01043-16
- SARS-CoV-2 – The Battle against Coronavirus has just Begun . https://lucerna-chem.ch/anti-covid-19-compounds
- de Wit, E., van Doremalen, N., Falzarano, D. et al. SARS and MERS: recent insights into emerging coronaviruses. Nat Rev Microbiol 14, 523–534 (2016). https://doi.org/10.1038/nrmicro.2016.81
- Durai, P., Batool, M., Shah, M. et al. Middle East respiratory syndrome coronavirus: transmission, virology and therapeutic targeting to aid in outbreak control. Exp Mol Med 47, e181 (2015). https://doi.org/10.1038/emm.2015.76
- Jiang, S., Du, L., & Shi, Z. (2020). An emerging coronavirus causing pneumonia outbreak in Wuhan, China: calling for developing therapeutic and prophylactic strategies. Emerging microbes & infections, 9(1), 275–277. https://doi.org/10.1080/22221751.2020.1723441
- https://www.who.int/ru/news-room/q-a-detail/coronavirus-disease-(covid-19)-vaccines?gclid=Cj0KCQjwutaCBhDfARIsAJHWnHuCclmgjC9qAJjhBkGmUCf_Ebq0OIcvB1XfHrLPU_o23DVfaA3rRGwaAsJqEALw_wcB&topicsurvey=v8kj13
- https://www.who.int/publications/m/item/moderna-covid-19-vaccine-(mrna-1273)
- https://www.modernatx.com/covid19vaccine-eua/
- https://www.who.int/ru/news-room/q-a-detail/coronavirus-disease-(covid-19)-vaccines?gclid=Cj0KCQjwutaCBhDfARIsAJHWnHuCclmgjC9qAJjhBkGmUCf_Ebq0OIcvB1XfHrLPU_o23DVfaA3rRGwaAsJqEALw_wcB&topicsurvey=v8kj13