ბაქტერიები და ვირუსები – ნაწილი II
Date: 27.05.2020 Author: ჯანო მარხულია ( J. Markhulia )
ვირუსები: შესავალი და მიმოხილვა
წინამდებარე სტატია წარმოადგენს სტატიათა ციკლის „ბაქტერიები და ვირუსები“-ს მე-2 ნაწილს (იხილე: ნაწილი I – ბაქტერიები , ნაწილი III – კორონავირუსები ), რომელიც მთლიანად ეთმობა ინფექციის გადამტან ისეთ აგენტებს როგორიცაა ვირუსები. აქ საუბარია ვირუსების აგებულებაზე, კლასიფიკაციაზე, მათ გავრცელებაზე და ა.შ. სტატიათა ციკლის ბოლო ნაწილი სრულად ეთმობა კორონავირუსებს, ყურადღება გამახვილებულია მსოფლიოში დღეს მძვინვარე კორონავირუსული დაავადების – COVID-19-ის გამომწვევ ინფექციურ აგენტ SARS-CoV-2-ზე.
1892 წელს, რუსი ბოტანიკოსი დიმიტრი ივანოვსკი (Dmitry Ivanovsky), რომელიც იკვლევდა თამბაქოს მოზაიკის დაავადების (tobacco mosaic disease (TMD)) გამომწვევს, ფილტრაციის სპეციალური მოწყობილობის მეშვეობით, მივიდა დასკვნამდე, რომ მან აღმოაჩინა დაავადების წყარო. საქმე იმაშია, რომ მცენარის დაავადების მიზეზად მიიჩნეოდა უცნობი ბაქტერია, აქედან გამომდინარე პასტერ– ჩემბერლენდის კერამიკის ფილტრს (Pasteur-Chamberland filter), რომელსაც ივანოვსკი იყენებდა TMD-ით ინფიცირებული თამბაქოს ფოთლების ექსტრაქტის გასაფილტრად, სითხიდან უნდა მოეშორებინა 0.2 მიკრონზე მეტი ზომის ნებისმიერი ბაქტერია (იმ დროისთვის ეს ფილტრი ითვლებოდა სითხეების ბაქტერიებისგან ულტრაფილტრაციის სტანდარტად). თუმცა გაფილტრულმა ექსტრაქტმა კვლავ გამოიწვია ჯანსაღი მცენარის დაავადება. ამის შემდეგ მსგავს კვლევაში ჩაერთო სხვა მეცნიერები, მათ შორის იყო ჰოლანდიელი მიკრობიოლოგი მარტინ ბეიერინკი (Martinus Willem Beijerinck), რომელმაც დამატებით აჩვენა, რომ პათოგენს შეუძლია რეპროდუქცია და გავრცელება მასპინძელი მცენარის უჯრედებში, თუმცა ბაქტერიების მსგავსად არ შეიძლება კულტივირება საკვებ არეში[7-8].
ბეიერინკი მიიჩნევდა, რომ დაავადების გამომწვევი აგენტი არსებობდა თხევადი სახით, შესაბამისად ასეთ სითხეს მან უწოდა „сontagium vivum fluidum“ – „დამასნეულებელი ცოცხალი სითხე“, რომელიც მოქმედებს როგორც „ბიოლოგიური შხამი“ [7-9]. შემდგომში, ეს გარემოება დაედო საფუძვლად დაავადების გამომწვევი მსგავსი აგენტებისთვის საყოველთაოდ ეწოდათ „ვირუსი“, რაც ლათინურად “Virus”– სწორედ შხამს ნიშნავს. მოგვიანებით, ბეიერნიკის ჰიპოთეზა ვირუსების თხევადი ბუნების შესახებ უარყოფილ იქნა ამერიკელი ვირუსოლოგის უენდელ სტენლის მიერ, რომელმაც ელექტრონული მიკროსკოპით პირველმა დამზირა ვირუსის ნაწილაკები.
დღემდე დაგროვილ მეცნიერულ ცოდნაზე დაყრდნობით ვირუსები შეიძლება განვმარტოთ როგორც სუბმიკროსკოპული (ოპტიკური მიკროსკოპისთვის უხილავი), გენეტიკური მასალისა და ცილის შემცველ არაუჯრედული ინფექციური აგენტი, რომელსაც რეპლიკაცია (გამრავლება) შეუძლია მხოლოდ ცოცხალი უჯრედის შიგნით [10-13]. ზემოთ თქმულიდან გამომდინარეობს, რომ ვირუსები პარაზიტირებენ, ანუ მათ გასავრცელებლად სჭირდებათ სხვა უჯრედები. სამეცნიერო ენაზე ასეთ ინფექციურ აგენტებს მოიხსენიებენ ობლიგატურ უჯრედშიდა პარაზიტებად (obligate intracellular parasite), ხოლო იმ უჯრედებს, რომლებშიც ვირუსი მრავლდება უწოდებენ მასპინძელ უჯრედებს. ვირუსები აინფიცირებს ყველა სახის ორგანიზმს, მცენარეებიდან და ცხოველებიდან დაწყებული, დამთავრებული ბაქტერიებით [12].
ცოცხალია თუ არა ვირუსი? როგორია მისი ევოლუციური წარმოშობის გზა? ეს ის კითხვებია, რაზეც მეცნიერებს ცალსახა პასუხი არ აქვთ და მსგავსი საკითხები ჯერ კიდევ რჩება დისკუსიის საგნად [8,10-14]. მართლაც, მეორე კითხვის პასუხად, არსებობს ვირუსების წარმოშობის სამი ძირითადი ჰიპოთეზა: რეგრესიული ჰიპოთეზა (regressive hypothesis), უჯრედული წარმომავლობის ჰიპოთეზა, რომელსაც უწოდებენ პროგრესულ ან გაქცევის ჰიპოთეზას (The progressive or escape hypothesis) და კოევოლუციური ჰიპოთეზა (Coevolution hypothesis) [16]. რაც შეეხება პირველ კითხვას, რადგანაც ვირუსებს აქვთ ზოგიერთი, მაგრამ არა ყველა ის ძირითადი მახასიათებელი ნიშან-თვისება (სუნთქვა, ზრდა, კვება, მოძრაობა და ა.შ), რაც გააჩნია ცოცხალ ორგანიზმებს, ვირუსები აღიწერება, როგორც „ორგანიზმები სიცოცხლის ზღვარზე“ და როგორც რეპლიკატორები [12,15]. უფრო გასაგები, რომ გახდეს ეს უკანასკნელი დასკვნა, საჭიროა ვირუსებზე საუბრისას გავიაზროთ ვირიონის ცნება.
როგორც აღვნიშნეთ, ვირუსს გასამრავლებლად სჭირდება მასპინძელ უჯრედში მოხვედრა. დაინფიცირების შემდეგ, მასპინძელი უჯრედი იძულებულია „აწარმოოს“ საწყისი ვირუსის ათასობით იდენტური ასლი. როდესაც ვირუსი არ იმყოფება დაინფიცირებული უჯრედის შიგნით ან მის დაინფიცირების პროცესშია, ასეთ დროს ის არსებობს დამოუკიდებელი ნაწილაკის – ვირიონის სახით.
აქედან გამომდინარე ვირიონი შეიძლება გაგებულ იქნას, როგორც ერთეული სტაბილური ვირუსული ნაწილაკი, რომელმაც დატოვა დაინფიცირებული უჯრედი და უნარი აქვს დააინფიციროს იგივე ტიპის სხვა უჯრედები [12-18].
ამრიგად, ვირუსი წარმოადგენს ზოგად ტერმინს მსგავსი ტიპის ინფექციური აგენტებისთვის, ანუ ის არის პარაზიტული აგენტების სახეობა, რომელსაც არ შეუძლია გამრავლება მასპინძელი უჯრედის გარეთ, მაშინ როდესაც ვირიონი წარმოადგენს ინფექციურ ნაწილაკს უჯრეთგარეთა ფაზაში [19]. ამ თვალსაზრისით ვირიონები, რომლებიც არსებობენ მასპინძელი-უჯრედის გარეთ და ასევე შეიძლება არსებობდნენ გარემოში, წარმოადგენს ინფექციურ ნაწილაკებს და არ შეიძლება ჩაითვალოს ცოცხალ ობიექტებად [15]. მხოლოდ მას შემდეგ რაც, ვირიონი მიებმება, შეიჭრება და გახდება უჯრედის ნაწილი, ის იძენს სასიცოცხლო მახასიათებლებს და მასპინძელი უჯრედის ბიოქიმიური პროცესების გამოყენებით ახდენს საკუთარი თავის რეპროდუქციას [14].
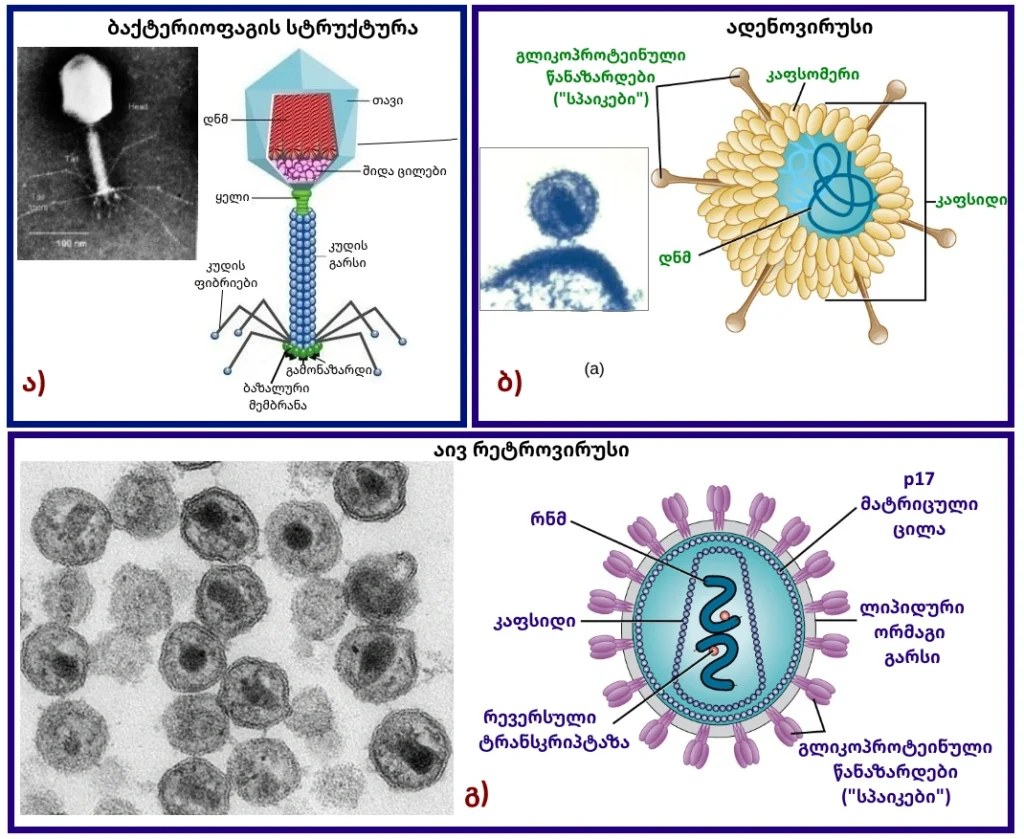
აქვე უნდა ავღნიშნოთ, რომ არსებობს ვირუსების ჯგუფი, რომლებიც შერჩევით აინფიცირებს, მასში მრავლდება და ანადგურებს მხოლოდ კონკრეტული ტიპის ბაქტერიულ უჯრედებს, ამ ჯგუფის ვირუსებს ბაქტერიოფაგებს უწოდებენ (სურ.1, ა)) [20].
2.1 ვირუსული ნაწილაკების აგებულება
ყველა ვირიონს აქვს ცილოვანი გარსი – ე.წ კაფსიდი, რომლის შიგნით მოთავსებულია გენეტიკური მასალა – დეზოქსირიბონუკლეინის მჟავის (დნმ) ან რიბონუკლეინის მჟავის მოლეკულა (მაგრამ არა ორივე ერთად), რომელიც ახდენს ცილის სტრუქტურის კოდირებას (სურ.1) [13, 19]. კაფსიდს, მასში მოთავსებული ნუკლეინის მჟასთან ერთად უწოდებენ ნუკლეოკაფსიდს. კაფსიდი შედგება ცილოვანი სუბერთეულებისგან – კაფსომერებისგან, რომელიც თავის მხრივ შედგება ერთი ან რამდენიმე სხვადასხვა ტიპის კაპსომერული ცილისგან, ეს ცილები ებმებიან ერთმანეთს და ქმნიან მჭიდროდ შეფუთულ გარსს [8]. კაფსიდი ვირუსის გენეტიკური მასალის ეფექტური დამცავი ბარიერია. უმეტეს შემთხვევაში ვირუსული ნაწილაკების ცილოვანი გარსები, ძალზე მყარია, დაახლოებით ისეთივე ძლიერი, როგორიც არის პლასტმასი ან ორგანული მინა, ამასთან ის არის ძალიან მცირე ზომის (ათეულ/ასეული ნანომეტრი). გარდა ამისა ვირუსების კაფსიდი გამოირჩევა ელასტიურობითა და უნარი აქვთ ფორმის მესამედით დეფორმაციის შემთხვევაშიც არ დაზიანდეს. სიმყარის, მოქნილობისა და მცირე ზომების ამგვარი კომბინაცია ნიშნავს, რომ ძალიან რთულია (თუმცა არა შეუძლებელი) ვირუსული ნაწილაკის დაშლა ფიზიკური ძალის ან წნევის ზემოქმედებით [10].
ზოგადი შემადგენლობის მიხედვით გამოყოფენ ორი კატეგორიის ვირუსულ ნაწილაკებს: 1) ვირიონები, რომლებიც შედგება მხოლოდ ნუკლეინის მჟავისა და კაფსიდისგან – მათ უგარსო ვირუსებს (nonenveloped/naked viruses) უწოდებენ (სურ.1 ბ)); და 2) ვირიონები, რომლებიც შედგება ნუკლეინის მჟავისა და ლიპიდური შრით დაფარული კაფსიდისგან – ასეთ ვირუსულ ნაწილაკებს გარსიანი ვირუსებს (enveloped viruses) უწოდებენ (იხ. სურ 1, დ) [8]. ამ ვირუსების დამატებითი მემბრანული გარსი „დამზადებულია“ მასპინძელი-უჯრედის მემბრანის მასალისგან, რაზეც უფრო დაწვრილებით ქვემოთ ვისაუბრებთ.

გარსიან და ზოგიერთ უგარსო ვირუსებს კაფსიდიდან მოშორებით გააჩნიათ გარეთა მხარეს მიმართული, გლიკოპროტეინული გამონაზარდებით (glycoprotein spike) – პეპლომერები. ეს გამონაზარდები (ზოგან მოიხსენიებენ „სპაიკებად“) უკავშირდება კონკრეტულ რეცეპტორების მქონე უჯრედებს და ამგვარად განსაზღვრავენ, რა ტიპის მასპინძელს ან მასპინძელ-უჯრედებს დაავადებს ესა თუ ის სახეობის ვირუსი და რამდენად მაღალი იქნება მისი ინფექციურობის ალბათობა (სურ. 1 ბ),გ)) [13, 18]. მაგალითად, გრიპის ვირუსი, ჰემაგლუტინინის (H) „სპაიკების“ მეშვეობით ახორციელებს სამიზნე უჯრედის ზედაპირის რეცეპტორთან შეკავშირებას და შიგნით შეღწევას, ხოლო ფერმენტების, როგორიცაა ნეირამინიდაზა (N) (რომელიც მსგავსია გრიპის ვირუსის „სპაიკის“), დახმარებით ახერხებს აწყობილი ვირიონების ინფიცირებული უჯრედიდან გამოთავისუფლებას [10-12]. გრიპის ვირუსების იდენტიფიცირებას ხშირად ახდენენ სწორედ H და N შტამების მეშვეობით. ასე მაგალითად, გრიპის ვირუსები H1N1 იყო 1918 და 2009 წლეში პანდემიის მიზეზი, ხოლო H2N2 და H3N2 შტამები, შესაბამისად 1957 და 1968 წლების – პანდემიების. ვირუსული ნაწილაკების ეს გარსები, როგორც ზემოთ აღინიშნა, იწყობა მასპინძელი უჯრედის მემბრანის კომპონენტებისგან (ფოსფოლიპიდებისა და ცილებისგან), ვირუსის რეპროდუქციის ციკლის იმ ეტაპზე, როდესაც ის ტოვებს მასპინძელ-უჯრედს [8, 19-22].
2.2 ვირუსების კლასიფიკაცია და ტაკსონომია
მიუხედავად იმისა, რომ ვირუსები, დედამიწაზე არსებული სიცოცხლის სამი დომენიდან (ბაქტერიები, ეუკარიოტები, არქეები) არც ერთს არ არიან მიკუთნებული, მათი რიცხვი იმდენად დიდია, რომ მოითხოვს კლასიფიკაციას [8].
ისტორიულად ვირუსების კლასიფიკაცია ხდებოდა სხვადასხვა მახასიათებელი ნიშნების მიხედვით, მათ შორის ფენოტიპური მახასიათებლებით, ქიმიური შემადგენლობით, კაფსიდის სტრუქტურით, ფორმით, გენომის სტრუქტურითა და რეპლიკაციის ხერხებით [23].
პირველ ორგანიზებულ მცდელობას, მოეწესრიგებინათ და კლასიფიცირებულად დაელაგათ სხვადასხვა სახეობის ვირუსები, რომელიც იქნებოდა საერთაშორისო, ადგილი ჰქონდა 1966 წელს მიკრობიოლოგიის საერთაშორისო კონგრესზე. ამავე წელს შეიქმნა შესაბამისი კომიტეტი, რომელსაც მოგვიანებით ეწოდა ვირუსების ტაქსონომიის საერთაშორისო კომიტეტი (ICTV). 1971 წლიდან მიკრობიოლოგიური საზოგადოების საერთაშორისო კავშირმა (IUMS) მიზნად დაისახა შეემუშავებინა ვირუსების უნივერსალური ტაქსონომია და შეეთავაზებინა ის ვირუსების ტაქსონომიის საერთაშორისო კომიტეტისთვის [8,24].
დღეისათვის არსებობს ვირუსების ნომენკლატურის ICTV ოფიციალური სისტემა და მისი ალტერნატივა ბალტიმორის კლასიფიკაცა. თუმცა ასევე არსებობს ვირუსების არაფორმალური კლასიფიკაციები [8].
ქვემოთ განვიხილავთ ვირუსების სხვადასხვა კლასიფიკაციის ვარიანტებს, მათი განსხვავებული კრიტერიუმების საფუძველზე.
2.2.1 კლასიფიკაციები ნუკლეინის მჟავების საფუძველზე
უჯრედული გენომისგან განსხვავებით, რომლებიც უნივერსალურად კოდირებულია ორჯაჭვიანი დნმ-ის (double-stranded DNA – dsDNA) ენაზე, ვირუსების გენომები საოცრად მრავალფეროვანია. ვირუსული გენომები შეიძლება იყოს ერთი- ან ორჯაჭვიანი დნმ ან რნმ ვერსიების სახით, რომლებიც „შეფუთულია“ სეგმენტებად ან ერთ ფრაგმენტად, ამასთან ასევე შესაძლებელია წარმოდგენილი იყოს როგორც წრფივი (ხაზოვანი) ისე რგოლური ფორმით [17,23]. ვირუსების გენომის ასეთი მრალაფეროვნება გახდა საფუძველი მათი ნუკლეინის მჟავების მიხედვით კლასიფიკაციისა.
2.2.1.1 დნმ ვირუსები
ამ ჯგუფის ვირუსებში გენეტიკურ მასალას წარმოადგენს დნმ. არსებობს ორი განსხვავებული ტიპის დნმ ვირუსები:
- ერთჯაჭვიანი დნმ-ვირუსები (Single-stranded DNA (ssDNA) viruses): მაგალითად პიკორნავირუსი (Picornavirus), პარვოვირუსი (Parvovirus) და სხვ.
- ორჯაჭვიანი დნმ- ვირუსები (Double-stranded DNA (dsDNA) viruses): მაგალითად ადენოვირუსი (Adenovirus), ჰერპესვირუსი (Herpesvirus) და სხვ.
2.2.1.2 რნმ-ვირუსები
ამ ჯგუფის ვირუსებს გენეტიკურ მასალად აქვთ რნმ. არსებობს ორი განსხვავებული ტიპის რნმ ვირუსი:
- ორჯაჭვიანი რნმ-ვირუსები (Double-stranded RNA (dsRNA) viruses): მაგალითად რეოვირუსი (Reovirus) და სხვ.;
- ერთჯაჭვიანი რნმ-ვირუსები (Single-stranded RNA (ssRNA) viruses). ისინი თავის მხრივ იყოფიან ორ ქვეჯგუფად რნმ დადებითი (+RNA) და რნმ უარყოფითი (-RNA). რნმ დადებით ვირუსებში (+) რნმ ჯაჭვი ასრულებს როგორც მემკვიდრულ ისე ინფორმაციული-რნმ-ს (ი-რნმ) ფუნქციას; ხოლო რნმ უარყოფით ვირუსებში (-) რნმ ჯაჭვი ასრულებს მხოლოდ მემკვიდრულ ფუნქციას [17,26]. პოლიოვირუსი (Poliovirus), A ჰეპატიტი, ცოფის ვირუსი წარმოადგენენ ერთჯაჭვიანი რნმ ვირუსების მაგალითებს [26].
2.2.2 ICTV კლასიფიკაცია
ვირუსების ტაქსონომიის საერთაშორისო კომიტეტი (International Committee on Taxonomy of Viruses – ICTV ) ვირუსების გენეტიკის, ქიმიის, მორფოლოგიის და გამრავლების მექანიზმების საფუძველზე, დღეისათვის ცნობილი ვირუსების კლასიფიცირებას ახდენს შვიდ რიგად, 96 ოჯახად და 350 გვარად [8,23].
ვირუსების ოჯახის სახელი მთავრდება viridae-ზე (მაგალითად Parvoviridae ) ხოლო გვარის დასახელება – virus-ით (მაგალითად Parvovirus ). ვირუსების რიგის, ოჯახის და გვარის სახელები იწერება კურსივით [8].
ამრიგად ICTV-ის მიხედვით გვაქვს ვირუსების შემდეგი შვიდი რიგი: Herpesvirales, ეუკარიოტული ორჯაჭვიანი დნმ (dsDNA) ვირუსები; Caudovirales ანუ კუდიანი (თავ-კუდიანი ) ორჯაჭვიანი დნმ-ვირუსები, რომლებიც აინფიცირებენ ბაქტერიებს; Ligamenvirales, ხაზოვანი (წრფივი) ორჯაჭვიანი ვირუსები, რომლებიც აინფიცირებენ არქეებს; Mononegavirales, მცენარეებისა და ცხოველების არასეგმენტირებული უარყოფითი (-) ერთჯაჭვიანი რნმ-ვირუსები; Nidovirales, ხერხემლიანების დადებითი (+) რნმ-ვირუსები; Picornavirales, ერთჯაჭვიანი რნმ-ვირუსები დადებითი ჯაჭვით, აინფიცირებენ მცენარეებს, მწერებსა და ცხოველებს; და ბოლოს Tymovirales, მცენარეების ერთნაწილიანი (multipartite) დადებითი ერთჯაჭვიანი რნმ ვირუსები [23].
2.2.3 ბალტიმორის კლასიფიკაცია
ბალტიმორის კლასიფიკაცია ყველაზე ხშირად გამოიყენება ვირუსების კლასიფიკაციის სისტემის შესასწავლად. კლასიფიკაციის ეს სქემა შემუშავდა ამერიკელი ბიოლოგის (ვირუსოლოგის) დევიდ ბალტიმორის ( David Baltimore) მიერ 1971 წელს, რომელიც ითვალისწინებს ვირუსის ნუკლეინის მჟავების ბუნებასა და რეპლიკაციის ხერხს [25].
ბალტიმორსეული კლასიფიკაციით ვირუსები ასევე დაჯგუფებულია 7 კატეგორიად (სურათი 2) ორჯაჭვიანი დნმ ვირუსები (I ჯგუფი); ერთჯაჭვიანი დნმ-ვირუსები (II ჯგუფი); ორჯაჭვიანი რნმ -ვირუსები (III ჯგუფი); დადებითი (+) ერთჯაჭვიანი რნმ – ვირუსები (IV ჯგუფი); უარყოფითი (-) ერთჯაჭვიანი რნმ -ვირუსები (V ჯგუფი); დადებითი ერთჯაჭვიანი რნმ -ვირუსები დნმ- ინტერმედიატებით (VI ჯგუფი), რომლებიც ასევე ცნობილია როგორც რეტროვირუსები; და ორჯაჭვიანი დნმ- რეტროვირუსები (VII ჯგუფი)

2.2.4 ვირუსების მასპინძელ დომენზე დაფუძნებული კლასიფიკაცია
ვირუსების მასპინძლების ტიპის მიხედვით გამოყოფენ ოთხ განსხვავებულ ჯგუფს [26].
2.2.4.1 ცხოველთა ვირუსები
ვირუსების ეს სახეობები აინფიცირებენ ცხოველებს, მათ შორის ადამიანებს, უჯრედში შეჭრის გზით. ცხოველთა ცნობილი ვირუსების მაგალითებია : გრიპის ვირუსი (influenza virus), ეპიდემიური პაროტიტის ვირუსი (mumps virus), ცოფის ვირუსი (rabies virus), პოლიოვირუსი (poliovirus), ჰერპესის ვირუსი (Herpes virus) და სხვ.
2.2.4.2 მცენარეული ვირუსები
ეს ვირუსები აინფიცირებენ მცენარეებს მათ უჯრედებში შეჭრით. მცენარეების ცნობილი ვირუსებია: კარტოფილის ვირუსი (potato virus), თამბაქოს მოზაიკური ვირუსი (tobacco mosaic virus), ყვავილოვანი კომბოსტოს ვირუსი (cauliflower mosaic virus) და სხვ.
2.2.4.3 ბაქტერიოფაგი
როგორც ზემოთ ავღნიშნეთ ეს ვირუსები აინფიცირებენ ბაქტერიულ უჯრედებს. არსებობს ბაქტერიოფაგების მრავალი სახეობა, ისეთები როგორიცაა T4 ბაქტერიოფაგი (Escherichia virus T4), M13 ბაქტერიოფაგი (M13 bacteriophage), λ-ფაგი (λ phage) და სხვ.
2.2.4.4 მწერების ვირუსები
ამ ჯგუფის ვირუსები აინფიცირებენ მწერებს, შესაბამისად მათ უწოდებენ მწერების ვირუსებს ან მწერების ვირუსულ პათოგენებს. ეს ვირუსები ითვლებიან თანამედროვე სოფლის მეურნეობის ლანშაფტის ბიოკონტროლის მძლავრ აგენტებად [26]. ამ ჯგუფის ვირუსების ცნობილი წარმომადგენლებია Ascovirus virions და Entomopox virus.
2.2.5 ვირუსების კლასიფიკაცია რეპლიკაციის ხასიათისა და განხორციელების ადგილის მიხედვით
ვირუსები იჭრებიან მასპინძელ-უჯრედში, სადაც ისინი რეპლიცირებენ და აიწყობიან უჯრედული ორგანელების შიგნით. ვირუსების რეპლიკაციის თავისებურებების მიხედვით მათ აჯგუფებენ შემდეგნაირად:
- რეპლიკაცია ხორციელდება მასპინძელი-უჯრედის ციტოპლაზმაში. მაგალითად, ყველა რნმ-ვირუსები, გარდა გრიპის ვირუსისა;
- რეპლიკაცია ხორციელდება მასპინძელი-უჯრედის ბირთვსა და ციტოპლაზმაში. მაგალითად, გრიპის ვირუსი (Influenza virus), პოქსვირუსი (Poxvirus) და სხვ;
- რეპლიკაცია ხორციელდება მასპინძელი-უჯრედის ბირთვში; ყველა დნმ-ვირუსები, გარდა პოქსვირუსისა;
- რეპლიკაცია ხორციელდება ორჯაჭვიანი შუალედური დნმ-ს მეშვეობით. მაგ. დნმ-ვირუსები, რეტროვირუსი და სიმსივნის გამომწვევი ზოგიერთი რნმ-ვირუსები;
- ვირუსების რეპლიკაცია ხორციელდება შუალედური ერთჯაჭვიანი რნმ-ს მეშევეობით. მაგ. ყველა რნმ-ვირუსები, გარდა რეოვირუსისა და სიმსივნის გამომწვევი რნმ-ვირუსებისა.
2.2.6 სტრუქტურაზე ან სიმეტრიაზე დაფუძნებული კლასიფიკაცია
ელექტრონულ მიკროსკოპიული კვლევებით დადგინდა, რომ სხვადასხვა სახეობის ვირუსებს აქვთ განსხვავებული ზომა, ფორმა და სტრუქურა. აღმოჩნდა, რომ ვირიონები განსხვავდებიან თავიანთი კაფსიდის ფორმით, რომლებსაც შეიძლება ჰქონდეთ სპირალური, მრავალწახნაგოვანი ან კომპლექსური ფორმები. სპირალურ კაფსიდს ქმნის თამბაქოს მოზაიკის ვირუსი (TMV), უგარსო სპირალური ვირუსი, სპირალური გარსიანი ვირუსი და ებოლა ვირუსი. ცილინდრული ან ჩხირისებრი კაფსიდის მქონე ვირუსებში გენომი მოთავსებულია გრძივად. მრავალწახნაგიან კაფსიდებს ქმნიან პოლიოვირუსები და რინოვირუსები, რომლებიც ნუკლეინის მჟავებს შეიცავენ იკოსაედრის ფორმის მქონე კაფსიდის შიგნით. იკოსაედრული კაფსიდი ეს არის სამგანზომილებიანი, 20 წახნაგიანი სტრუქტურა 12 წვეროთი. ასეთი კაფსიდები მოგვაგონევს ფეხბურთის ბურთს [17,27-28].
როგორც სპირალურს ისე მრავალწახნაგოვან ვირუსებს შეიძლება ჰქონდეთ გარსები. ზოგიერთი ტიპის ბაქტერიოფაგების ვირიონებს, ისეთებს როგორიცაა Т4 და პოქსივირუსებს, როგორიცაა ყვავილვაქცინის ვირუსი (vaccinia virus), შეიძლება გააჩნდეთ, როგორც მრავალწახნაგური ისე სპირალური ვირუსების დამახასიათებელი ფორმები, ამიტომაც ასეთი ვირუსები აღიწერებია როგორც რთული (კომპლექსური) ვირუსული ფორმა [26-27]. კერძოდ ცხოველების ვირუსების ვირიონთა უმრავლესობას აქვს იზომეტრული იკოსაედრული სტრუქტურები ან სფეროსებრი ცილოვანი კომპლექსები, რომლებიც გარედან შემოსაზღვრულია ლიპიდშემცველი გარსით[18].
ვირიონთა ასეთი მრავალფეროვნების გამო არსებობს ვირუსების ალტერნატიული კლასიფიკაცია, რომელიც ეფუძნება ვირუსების დაჯგუფებას მათი ვირიონების სტრუქტურისა და სიმეტრიის შესაბამისად [26]. ამ სქემის მიხედვით ვირუსები დაჯგუფებულია შემდეგნაირად:
- (1) რთული ვირუსები. მაგალითად ნატურალური ყვავილი (Poxvirus);
- (2) რადიალური სიმეტრიის ვირუსები. მაგ. ბაქტერიოფაგი;
- (3) კუბური ან იკოსაედრული სიმეტრიის ვირუსები, მაგალითად რეოვირუსი (Reovirus), Picornavirus;
- (4) ჩხირისებრი ან სპირალური სიმეტრიის ვირუსები. მაგალითად , პარამიქსოვირუსი (Paramyxovirus), ორთომიქსოვირუსი (orthomyxovirus)
აქვე შევნიშნოთ, რომ კვლევებით გამოიკვეთა საინტერესო თავისებურება, კერძოდ ვირიონის მორფოლოგიის სირთულე კორელაციაში არ არის მისი მასპინძლის სირთულეში. მართლაც ყველაზე რთული სტუქტურები დაიმზირება უმატრივესი ორგანიზმების – ბაქტერიების ვირუსებში ანუ ბაქტერიოფაგებში [21].
სურათ 3-ზე წარმოდგენილია სხვადასხვა სახეობის ვირუსების ვირიონების ფორმისა და ზომის გრაფიკული ილუსტრაცია.

ქვემოთ ასევე შეგიძლიათ იხილოთ სხვადასხვა ფორმის ვირუსების ვიდეოანიმაცია.
2.3. ვირუსების გამრავლება
რადგანაც ვირუსები წარმოადგენენ უჯრედშიდა პათოგენებს, მათ არ შეუძლიათ რეპლიკაცია მასპინძელი უჯრედის მეტაბოლიზმის მექანიზმის გარეშე. შესაბამისად, ბაქტერიებისგან განსხვავებით ვირუსები არ მრავლდებიან გაყოფის გზით, არამედ აიწყობიან მასპინძელი უჯრედის მიერ წინასწარ დამზადებული კომპონენტებისგან, ამასთან მათ არ შეუძლიათ გამოიმუშაონ ენერგია და აწარმოონ საკუთარი ცილები [30].
ვირუსით დაინფიცირებული უჯრედი ჰგავს ფაბრიკას, რომელიც აწარმოებს ვირიონებს. სწორედ ეს გარემოებები ბადებს კითხვას ვირუსის როგორც ცოცხალი ორგანიზმის თაობაზე. გამოდის, რომ მასპინძელი უჯრედის შიგნით ვირუსები ცოცხალია, მაშინ როდესაც მის გარეთ, ისინი წარმოადგენენ მხოლოდ და მხოლოდ მეტაბოლურად ინერტული ქიმიური ნივთიერების რთულ კომპლექსს [10,14].
2.3.1 ვირუსის სასიცოცხლო ციკლი
ვირუსის რეპლიკაცია მოითხოვს მასპინძელ-უჯრედთან სფეციფიკურ ურთიერთქმედებას. რეპლიკაციის ციკლი იწყება ვირუსული ცილების მასპინძელ-უჯრედის რეცეპტორებთან მიმაგრებით. შესაბამისი რეცეპტორების არსებობა ან არარსებობა წარმოადგენს საკვანძო ფაქტორს, რომელიც განსაზღვრავს დაინფიცირებადია ეს უჯრედი ამ კონკრეტული ვირუსის მიერ თუ არა. რეპლიკაციის ციკლის შემდეგ ეტაპს წარმოადგენს გენომის გადატანა ციტოზოლში ან ნუკლეოპლაზმაში. ზოგიერთი ვირუსის მასპინძელ-უჯრედში ახდენს მხოლოდ თავისი გენომის ტრანსპორტირებას, ზოგი კი – მთლიანი ვირიონის. უჯრედში მოხვედრის შემდეგ ვირიონული ცილები და გენომი ურთიერთქმედებენ სხვადასხვა უჯრედულ ცილებთან, ნუკლეინის მჟავებთან და მემბრანებთან. წარმატებული რეპლიკაციისთვის საჭიროა განხორციელდებს ვირუსული ი-რნმ-ს, ცილებისა და გენომების სინთეზი [18,29]. {ამ პროცესების მექანიზმები ძლიერ განსხვავდება ერთმანეთისგან. თუმცა იმისათვის, რომ ვირუსმა მიაღწიოს წარმატებას, მან კონკურენცია უნდა გაუწიოს მასპინძელ-უჯრედს და მისი ძირითადი ფუნქციის პარალელურად შეასრულებინოს ვირუსის სასარგებლო სამუშაოები}.
ვირუსის სასიცოცხლო ციკლის პარაზიტული ფაზა იწყება ვირუსული გენომის მასპინძელ უჯრედში მოხვედრისთანავე [18]. ვირუსებს თავისთავად არ შეუძლია ყველა იმ ფერმენტის კოდირება, რომელიც აუცილებელია ვირუსის რეპლიკაციისთვის, მაგრამ მასპინძელი უჯრედის შიგნით მას შეუძლია უჯრედული მექანიზმის მართვა. ბაქტერიული ვირუსები (ბაქტერიოფაგები) რეპლიცირდება მხოლოდ ციტოპლაზმაში, რამდენადაც პროკარიოტულ უჯრედებს არ გააჩნიათ ბირთვი ან ორგანოიდები. ეუკარიოტულ უჯრედებში დნმ-ვირუსების უმრავლესობას შეუძლია რეპლიცირება ბირთვის შიგნით, გამონაკლისს წარმოადგენს გიგანტური დნმ ვირუსები (Giant viruses), რომლებიც რეპლიცირდებიან ციტოპლაზმაში. რნმ-ვირუსები, რომლებიც აინფიცირებენ ცხოველურ უჯრედებს, რეპლიკაციას უმეტესად ახორციელებენ ციტოპლაზმაში [8,17]. ეს ვირუსები გამოირჩევიან რეპროდუქციის სპეციფიკური, ე.წ წყვეტილი (disjunctive) მეთოდით: მასპინძელ უჯრედში ცალ-ცალკე ხდება ნუკლეინის მჟავებისა და ცილების სინთეზი, ხოლო შემდეგ ხდება მათი აწყობა ვირუსულ ნაწილაკებად (ვირიონად) [31].
ამრიგად ვირუსის სასიცოცხლო ციკლი მოიცავს ვირუსული გენეტიკური მასალის მასპინძელ-უჯრედში მოხვედრას (ვირუსის გადაცემა), ამ მასალის რეპლიკაციას და ახალი ვირუსების უჯრედიდან გამოთავისუფლებას [33].
სანამ უშუალოდ დეტალურად განვიხილათ სასიცოცხლო ციკლის ყოველ სტადიას, ზოგადად განვიხილოთ უჯრეთგარეთა სივრცე, კერძოდ ვისაუბროთ უჯრედშორის მატრიქსზე (უგმ) და უჯრედის პლაზმური მემბრანაზე.
2.3.2 უჯრედგარეთა სივრცე
ცხოველური უჯრედების უმრავლესობა მოქცეულია უჯრედგარეთა მატრიქსში (უგმ) (ასევე მოიხსენიებენ უჯრედშორის მატრიქსად – extracellular matrix) რომელიც ასევე დიდ როლს ასრულებს ქსოვილებისა და ორგანოების ჩამოყალიბებაში. უჯრედშორისი მატრიქსის დიდი ნაწილი თავისი ბუნებით ცილოვანი წარმოშობისაა; თუმცა ეპითელური უჯრედების შემთხვევაში პლაზმური მემბრანა (პმ) შემოსაზღვრულია პოლისაქარიდების ფენით, რომელიც იწოდება გლიკოკალიქსად. ამრიგად, ინფექციურმა აგენტებმა (ვირუსებმა) სანამ ისინი მიაღწევენ უშუალოდ უჯრედამდე უნდა გაიარონ ეს უჯრედშორისი სივრცე (არე), ანუ მოუწევთ იურთიერთქმედონ უჯრედშორისი მატრიქსის მოლეკულებთან, ამ არის გავლის შემდეგ შეძლებენ მოხვდნენ პლაზმურ მემბრანასთან (პმ). გამოდის, რომ გლიკოკალიქსი თითქოს წარმოადგენს ბარიერს უცხო სხეულისთვის, თუმცა ზოგიერთი ვირუსი სწორედ მას იყენებს თავის სასარგებლოდ და მის პოლისაქარიდებთან ამყარებენ მოლეკულურ კავშირებს [29].
უჯრედის ზედაპირი, კერძოდ კი პლაზმური მემბარნაც ასრულებს კიდევ ერთი, მორიგი ბარიერის როლს „დაუპატიჟებელი სტუმრებისთვის“, თუმცა ვირუსები ვითარებას აქაც ცვლიან თავიანთ სასარგებლოდ. კერძოდ, უჯრედის პლაზმურ მემბრანას იყენებენ კონკრეტულ უჯრედებთან სელექციურად (შერჩევით) მისამაგრებლად, მის ზედაპირზე „მსუბუქად დასაშვებად“ და შემდეგ ეტაპზე მის შიგნით შესაღწევად.
ამ საკითხების უკეთ გასაგებად საჭიროა გავერკვეთ თუ რა არის პლაზმური მემბარანა და როგორია მისი სტრუქტურა. პმ წარმოადგენს შერჩევითად შეღწევად (განჭოლად) ლიპიდურ ბიშრეს, რომელიც შეიცავს ბევრ ცილას; ის არის რთული და დინამიური სტრუქტურა. მცირე მოლეკულები, ისეთები როგორიცაა ნახშიროჟანგი და ჟანგბადი, პლაზმურ მემბრნას განჭოლავენ დიფუზიის გზით. საქაროზა და ამინომჟავები მასში აღწევენ, ცილოვანი არხებისა და ტრანსპორტერების მეშვეობით. ხოლო უფრო დიდი მოლეკულების უჯრედში შესაღწევად საჭიროა განხორციელდეს ამ უკანასკნელთა ენდოციტოზი. პლაზმურ მემბრანასთან ასოცირებული ცილები, შეიცავენ რეცეპტორებს, სასიგნალო მოლეკულებს, ფერმენტებს და ადგეზიურ ცილებს (Cell Adhesion Proteins). როგორც სურ. 4-ზეა ნაჩვენები, პლაზმურ მემბრანასთან დაკავშირებულ ზოგიერთი ცილას გააჩნია ციტოპლაზმატური, მემბრანული და უჯრეთგარეთა დომენები, მაშინ როდესაც დანარჩენები მთლიანად ჩაშენებულია ბიშრეში. ცილები პმ-ში მოძრავია, ისინი მოძრაობენ ლატერალურად მემბრანის გავლით, მათ შეუძლიათ რეორგანიზება და სიგნალების გადაცემის შედეგად კომპლექსების წარმოქმნა. პლაზმური მემბრანის ცილები ხშირად გლიკოლიზირებულია (ნახშირწყლიანი ჯაჭვები მიერთებულია ცილის ძირითად ჯაჭვთან). სწორედ ზემოთ განხილულ სტრუქტურას და მოლეკულებს იყენებს ვირუსი უჯრედიში შესაღწევად [29].

ძირითადი თემიდან ასეთი მცირედი გადახვევის შემდეგ, კვლავ დაუბრუნდეთ ვირუსის სასიცოცხლო ციკლის სტადიებს და განვიხილოთ ისინი უფრო დაწვრილებით.
2.3.3 ვირუსის მასპინძელ უჯრედში მოხვედრა
ვირუსის სასიცოცხლო ციკლის პირველ ეტაპს წარმოადგენს მისი მასპინძელ-უჯრედში მოხვედრა (ვირუსული ნაწილაკის გადაცემა). ვირუსები, თავიანთი თავის გასავრცელებლად მთლიანად დამოკიდებული არიან მასპინძელ ორგანიზმზე. უმრავლეს შემთხვევაში მასპინძელი-ორგანიზმის ცალკეულ აქტივობებს (მოქმედებებს) პირდაპირ გადააქვს ვირუსი ერთიდან სხვა ორგანიზმზე. ზოგიერთი ვირუსი ახალ მასპინძელთან გადადის ვექტორის (ორგანიზმი, რომელიც ხელს უწყობს ინფექციის გადაცემას ერთი მასპინძლიდან მეორეზე, მაგ.როგორიცაა კოღო და სხვ.) მეშვეობით. ცხოველებსა და მცენარეებში ვირუსების გადაცემა უჯრედიდან უჯრედში ხდება საკუთრივ ორგანიზმში, ასევე გადაეცემა ახალ მასპინძელსაც. წარმატებული გადაცემა ნიშნავს, ვირუსის მოხვედრას არადაინფიცირებულ მასპინძელ-უჯრედში. უმრავლესი სახეობის ვირუსებითვის ეს ნიშნავს, რომ ვირუსმა უნდა შეაღწიოს ორგანიზმში და შემდეგ გადატანილ იქნას იმ კონკრეტულ უჯრედებში, რომელთა დაინფიცირება მას შეუძლია [34].
მიუხედავად იმისა, რომ ვირუსების რეპლიკაციური სასიცოცხლო ციკლი სხვადასხვა სახეობის ვირუსებში განსხვავებულია, არსებობს ექვსი ძირითადი ეტაპი, რომელიც აუცილებელია ვირუსის რეპლიკაციისთვის, ესენია: მიბმა (ადსორბცია), შეღწევა, გარსის მოხსნა/გენეტიკური მასალის გამოთავისუფლება, რეპლიკაცია (ვირუსული გენეტიკური მასალისა და ცილების სინთეზი), აწყობა და უჯრედიდან გამოსვლა (გამოთავისუფლება) [30,33]. ქვემოთ უფრო დაწვრილებით განვიხილავთ ამ ეტაპებს.
2.3.3.1 ვირუსის მასპინძელ-უჯრედთან მიბმა (ადსორბცია)
ვირიონის მასპინძლ-უჯრედთან მიბმა[1] (შეკავშირება) ხორციელდება მის კაფსიდზე არსებული მიმმაგრებელი ცილების (attachment proteins) ან ვირუსული გარსის გლიკოპროტეინების (ე.წ „სპაიკების“), მასპინძელი უჯრედის ზედაპირის ისეთ სპეციფიკურ მოლეკულებთან (რეცეპტორებთან), როგორიცაა მემბრანული ცილები, ლიპიდები ან ნახშირწყლების ფრაგმენტები (გლიკოლიპიდები ან გლიკოპროტეინები), შეკავშირებით. შესაბამისად თუ უჯრედს არ გააჩნია შესაბამისი რეცეპტორები მაშინ ვირუსი მასზე არ რეაგირებს. სწორედ ეს სპეციფიკურობა (კომპლიმენტარობა) განსაზღვრავს თუ რომელი მასპინძელი უჯრედების დაინფიცირება შეეძლება ვირუსს ანუ განსაზღვრავს ვირუსის მასპინძლების დიაპაზონს (ტროპიზმს). ვირუსების შერჩევითი დაინფიცირების მექანიზმის გაგება გამარტივდება, თუ გავავლებთ პარალელს და წარმოვიდგენთ რამდენიმე ციხესიმაგრეს და ამდენივე გასაღებს, სადაც ყოველი გასაღები შეესაბამება (აღებს) მხოლოდ ერთ კონკრეტულ ციხესიმაგრეს [30-38]. აქვე უნდა გვესმოდეს, რომ ვირუსებს არ შეუძლია კონკრეტული რეცეპტორის (სამიზნე მოლეკულის) მოძებნა. ისინი ასე ვთქვათ შემთხვევითად გადაადგილდებიან მასპინძელი ორგანიზმის უჯრედებს შორის და ასევე შემთხვევით ხვდებიან იმ უჯრედების გარემოცვაში, რომელთა დაინფიცირება მათ შეუძლიათ. {მიუხედავად იმისა, რომ ვირუსის მიერ უჯრედის დაინფიცირება ატარებს ალბათურ ხასიათს, მასპინძელ ორგანიზმში მის მოხვედრის შემდეგ ეს ალბათობა საკამაოდ დიდია}.
[1] ბმა ხორციელდება იონური ურთიერთქმედების შედეგად, რომელიც არ არის დამოკიდებული ტემპერატურაზე.
მასპინძელი უჯრედის სამიზნე მოლეკულასთან მიბმა განაპირობებს შემდგომში გენომის შეღწევას საკუთრივ უჯრედში, აღძრავს რა უჯრედშიდა სასიგნალო გზებს ან მასპინძელ-უჯრედებს საშუალებას აძლევს ვირიონი გადაიტანონ კონკრეტულ ორგანოში [38].
ვირუსის უჯრედული რეცეპტორები შეიძლება დაიყოს ორ კლასად: ადგეზიისა და შემყვან რეცეპტორებად. ადგეზიის რეცეპტორები (Adhesion receptors) უზრუნველყოფენ ვირიონის მიმაგრებას სამიზნე-უჯრედებთან ან ორგანოებთან. ეს ადგეზია არ წარმოადგენს აუცილებელ პირობას ვირუსის შესაღწევად და თავისთავად არ იწვევს შეღწევას, თუმცა ის მნიშვნელოვნად ზრდის დაინფიცირების ალბათობას, ახდენს რა ვირუსის კონცენტრირებას მის უჯრედში შემყვანი რეცეპტორებთან (entry receptors) მახლობლობაში (სურ.5). სწორედ შემყვანი რეცეპტორები რთავენ, ვირუსის, უჯრედში ენდოციტოზის მეშვეობით შეტანის რეჟიმს [38].

ა) სურათზე წარმოდგენილია გარსიანი ვირუსი გლიკოპროტეინული გამონაზარდებით („სპაიკებით“); „სპაიკებს“ გააჩნიათ უჯრედულ რეცეპტორებთან კომპლიმენტარული საცმი. პროცესს, რომლის დროსაც ვირუსი ხვდება უჯრედში და შეკავშირდება რეცეპტორებთან უწოდებენ მიმაგრებას (docking); ბ) უჯრედის ზედაპირზე რეცეპტორების სიმკვრივე და მიმაგრების ალბათობა; მეტი სიმკვრივის ან რაოდენობის (სხვადასხვა სახის) რეცეპტორების მქონე უჯრედების დაინფიცირება უფრო მეტად ალბათურია.
ვირუსის უჯრედის ზედაპირთან მიბმის პროცესში, როგორც აღინიშნა მონაწილეობს რამდენიმე ამინომჟავა ან ნახშირწყლების ფრაგმენტი. ამ პროცესისას მოლეკულებს შორის ურთიერთქმედება ელექტროსტატიკური ბუნებისაა და შესაბამისად საწყის ეტაპზე ვირუსისა და რეცეპტორების კონტაქტი სუსტი და შექცევადი ხასიათისაა. თუმცა, რამდენადაც ვირუსს კაფსიდზე (ან გარსზე) გააჩნია მიმაგრების ცილების საკმაოდ დიდი რაოდენობა და ამასთან, ისინი უმრავლეს შემთხვევაში ურთიერთქმედებენ არა ერთ, არამედ რამდენიმე ტიპის მოლეკულურ რეცეპტორთან, მიბმის პროცესი ძლიერდება და ხდება შეუქცევადი. აქედან გამომდინარე, უჯრედები რომლებიც გამოირჩევიან რეცეპტორების უფრო მეტი სიმკვრივით (სიმჭიდროვით) ან რაოდენობით უფრო ადვილად ექვემდებარებიან დაინფიცირებას (სურ5. ბ)) [29]. {შევნიშნოთ, რომ, რადგან ბმა ელექტროსტატიკურია, მასზე შეიძლება იმოქმედოს უჯრედგარეთა სივრცში არსებულმა pH მაჩვენებელმა, იონების ტიპმა და კონცენტრაციამ}.
2.3.3.2 ვირუსის მასპინძელ-უჯრედში შეღწევა
მას შემდეგ, რაც ვირუსი მიებმება უჯრედს, მომდევნო კრიტიკულ ეტაპს წარმოადგენს ვირუსული გენომის ციტოპლაზმაში ან ნუკლეოპლაზმაში მიწოდება (მიტანა). სხვადასხვა ვირუსი ამ მიზნის მისაღწევად იყენებს განსხვავებულ სტრატეგიებს [29].
მასპინძელი უჯრედის კონკრეტულ რეცეპტორთან მიბმის პროცესს შეუძლია გამოიწვიოს კონფორმაციული ცვლილებები ვირუსის კაფსიდის ცილებში ან ლიპიდურ გარსზე, რაც თავის მხრივ იწვევს ვირუსული და უჯრედული მემბრანების შერწყმას (იხ.სურ.6 ა)). შერწყმისას ვირუსი ან უშუალოდ გადადის ციტოპლაზმაში და „შეერევა“ უჯრედს, ან ეხვევა უჯრედული მემბრანის ბუშტუკში (ვეზიკულაში) – უჯრედშიდა მშთანთქმელ ორგანელაში (მაგალითად – ენდოსომაში) (სურ 6. ბ-3). ამ დროს, ვირუსი ჯერ კიდევ არ არის აქტიური. უჯრედში ასეთი სახით შეღწევა ძირითადად ახასიათებთ გარსიან ვირუსებს[2][33-34].
ზოგიერთ ვირუსს (ძირითადად უგარსო ვირუსებს), როგორც ავღნიშნეთ, შეუძლია მასპინძელ-უჯრედში შეაღწიოს ენდოციტოზის მეშვეობით. ამ დროს კონკრეტულ უჯრედულ რეცეპტორთან ბმული ვირიონი, უჯრედში აღძრავს სიგნალს, რის შემდეგაც უჯრედული მემბრანა გარს ერტყმის და ამგვარად უჯრედს შიგნით მოიქცევს ამ უკანასკნელს. ამრიგად, ფაქტობრივად ვირიონი, აიძულებს უჯრედს შთანთქოს და შეიყვანოს ის უჯრედს შიგნით (ამ პროცეს ასევე მოიხსენიებენ როგორც რეცეპტორ-დამოკიდებული ენდოციტოზს) (იხ.სურ.6 ბ)) [30,35].

ვირუსულ ინფექციებზე მომუშავე მეცნიერებისთვის ძალზე მნიშვნელოვანი და ღირებულია საკვლევი ვირუსის უჯრედში შეღწევის მექანიზმის დეტალური ცოდნა, რადგან დაინფიცირება შეიძლება თავიდან აცილებული იქნას თუ რაიმე გზით (საშუალებით) განხორციელდება ვირუსული გარსის უჯრედთან ან ენდოსომიალურ მემბრანასთან შერწყმის დაბლოკვა. ზუსტად ასევე, თუკი შევძლევთ ვაქცინის მიმართვას ვირუსის მიმაგრებელი (უჯრედთან შემრწყმელი) ცილისკენ და მოვახდენთ მის ინაქტივაციას, ასევე მოხერხდება დაინფიცირების თავიდან აცილება (სწორედ ამ უკანასკნელ გზას იყენებენ გრიპის ვაქცინის შემხვევაში).
რაც შეეხება ბაქტერიული ვირუსებს – ბაქტერიოფაგებს, მათი გენეტიკური მასალა მასპინძელ-უჯრედში აღწევს შემოუგარსავი სახით, ტოვებს რა კაფსიდს უჯრედს გარეთ (იხ.სურ. 6 გ) [30-34].
[2] ზოგიერთი გარსიანი ვირუსის უჯრედთან შერწყმისთვის აუცილებელია მჟავა pH გარემო, ამიტომაც მათ არ შეუძიათ პლაზმურ მემბრანასთან უშუალოდ შერწყმა. ეს ვირუსები შთაინთქმებან მემბრანის ინვაგინაციით ენდოსომების სახით (ენდოციტოზის გზით).
2.3.3.3 გარსის მოხსნა/გენეტიკური მასალის გამოთავისუფლება
მას შემდეგ, რაც ვირუსი შეიჭრება მასპინძელ-უჯრედში, იწყება ახალი სტადია, რომლის დროსაც გარსი და კაფსიდი იშლება და ვირუსული გენომი გამოთავისუფლდება შიდაუჯრედულ სითხეში (სურ.5 ა-4, ბ-5). ვირუსული რეპლიკაცია ვერ განხოლციელდება ამ ეტაპის გარეშე. აღმოჩნდა, რომ მას შემდეგ რაც ვირუსული ნაწილაკი გათავისუფლდება გარსისგან, ძალიან რთულია ვირუსული გენომის მასპინძელ-უჯრედში პოვნა, შესაბამისად ვერც ინფექციური ვირუსული ნაწილაკების „ამოღებაა“ შესაძლებელი ამ უჯრედიდან. მეცნიერებმა სტადიის ამ ეპიზოდს უწოდეს გაუჩინარების ფაზა (eclipse phase), ეს ფაზა გრძელდება ახალი ვირიონების აწყობამდე. აქვე უნდა აღინიშნოს, რომ ამ ეტაპზე უჯრედს შეუძლია ვირუსის განადგურება, ვირუსული შემოტევებისგან თავდაცვის ფერმენტებისა და შესაბამისი ფუნქციით აღჭურვილი მოლეკულების გამოყენებით. უჯრედები ვირუსებს უტევენ, ცილებისა და ნუკლეინის მჟავების გამოყენებით, რომლებიც გადაამუშავებენ ვირუსულ გენეტიკურ მასალას [32-34].
2.3.3.4 რეპლიკაცია (ვირუსული გენეტიკური მასალისა და ცილების სინთეზი)
ვირუსის სასიცოცხლო ციკლის ამ სტადიაზე ხორციელდება სინთეზი. კერძოდ, ვირუსი მასპინძელ-უჯრედს იყენებს ვირუსული გენომისა და კაფსომერების რეპლიკაციითვის. უხეშად რომ ვთქვათ, ვირუსის თავის გენეტიკურ მასალას იყენებს მასპინძელი-უჯრედის ორგანოიდების, უმრავლეს შემთხვევაში რიბოსომების „დასამონებლად“. სწორედ რიბოსომებია ის უჯრედული სტრუქტურები, რომლებიც აწარმოებენ ცილებს. მაშასადამე, მასპინძელი უჯრედისთვის საჭირო ცილების ნაცვლად, აწ უკვე „დამონებული“ უჯრედი ქმნის ვირუსისთვის აუცილებელ ცილებს. უჯრედში მყოფი ვირუსი ასევე იყენებს მასპინძელი-უჯრედის სხვა ისეთ კომპონენტებს, როგორიცაა ატფ (ადენოზინტრიფოსფორმჟავა), ენერგიის მისაღებად, სხვა საჭირო ამინომჟავებსა და ცხიმებს, ახალი კაფსიდის ასაწყობად [10,22].
რეპლიკაციის მექანიზმი მრავალგვარია და ის დამოკიდებულია ვირუსის ტიპზე [33-34]. ყოველი ვირუს გააჩნია მისთვის დამახასიათებელი (სფეციფიკური) სინთეზის სტადია, რომელიც დამოკიდებულია მის გენომის შემადგენლობაზე და კაფსიდის ტიპზე. ვირუსული გენომი არის ძირითადი ბაზისი ვირუსული კომპონენტების შესაქმნელად [32,34]. საერთო ჯამში, ვირუსების უმრავლესობა სინთეზის სტადიას იწყებს რეპრესორული ცილების (repressor proteins) წარმოებით, რომლებიც აკონტროლებენ მასპინძელი-უჯრედის განსაზღვრულ ფუნქციებს. ამ მომენტიდან უჯრედი უკვე დაავადებულია და ვერ ასრულებს თავის სასიცოცხლოდ მნიშვნელოვან ფუნქციებს. ამ სტადიაზე ზოგიერთი უჯრედი ნაადრევად იღუპება და, თავის მხრივ აჩერებს ვირუსის რეპლიკაციას. ადამიანებში, ინფიცირებული უჯრედები ჩვეულებრივ გამოიმუშავებენ სასიგნალო ცილებს, რომლებიც იწვევენ იმუნური პასუხის ინიცირებას, რომელიც მიმართულია ვირუსული რეპლიკაციის გაკონტროლებაზე [34]. დნმ-ვირუსები ჩვეულებრივ იყენებენ მასპინძელი-უჯრედის ცილებსა და ფერმენტებს, დამატებითი დნმ-ის მისაღებად, რომელიც ტრანსკრიბირდება ინფორმაციულ რნმ-ში (ი-რნმ), რომელიც შემდეგ გამოიყენება ცილის სინთეზის სამართავად. რნმ-ვირუსები, გენომური რნმ-სა და ი-რნმ-ს სინთეზისთვის იყენებენ რნმ-ს ბირთვს მატრიცის სახით. ვირუსული ი-რნმ მიმართავს მასპინძელ-უჯრედს და აიძულებს ასინთეზიროს ვირუსული ფერმენტები და კაფსიდური ცილები. რა თქმა უნდა განხილული სქემა წარმოადგენს ზოგადს და ის შეიძლება განსხვავდებოდეს ცალკეული ვირუსებისთვის. მაგალითად თუ მასპინძელი-უჯრედი ვერ უზრუნველყოფს ყველა აუცილებელ ფერმენტს ვირუსის რეპლიკაციისთვის, მაშინ ვირუსული გენები უჯრედს აწვდიან ინფრომაციას დანაკლისი ცილების პირდაპირი სინთეზისთვის. რეტროვირუსებს, როგორიცაა აივ, აქვთ რნმ-გენომი, რომელიც უნდა იქნას უკუტრანსკრიბირებული დნმ-ში, რომელიც ამის შემდეგ ჩაშენდება მასპინძელი-უჯრედის გენომში [32-34]. {რნმ-ს დნმ-ში გარდასაქმნელად, რეტროვირუსები, უნდა შეიცავდნენ გენებს (რადგან ამ გენებს არ შეიცავს ადამიანი უჯრედი), რომლებიც აკოდირებენ ვირუს-სფეციფიკურ ფერმენტს უკუტრანსკრიპტაზას. სწორედ ეს ფერმენტი ახდენს რნმ- მატრიცის დნმ-ში ტრანსკრიბირებას. უკუ ტრანსკრიფცია არასოდეს არ ხდება არაინფიცირებულ მასძპინძელ-უჯრედში; აუცილებელი ფერმენტი, უკუტრანსკრიპტაზა, წარმოიშობა (მომდინარეობს) მხოლოდ ინფიცირებულ მასპინძელ-უჯრედებში ვირუსული გენების ექსპრესიის შედეგად. ის ფაქტი, რომ აივ- აწარმოებს ზოგიეთ საკუთარ ფერმენტს, რომელიც არ მოიპოვება მასპინძელ-უჯრედში, საშუალებას აძლევს მკვლევარებს შეიმუშავონ წამლები, რომლებიც ამ ფერმენტების ინჰიბირებას ახდენენ. ეს პრეპარატები, მათ შორის, უკუტრანსკრიპტაზას ინჰიბიტორი AZT, ინჰიბირებენ აივ რეპლიკაციას, ფერმენტის აქტივობის შემცირებით, მასპინძლის მეტაბოლიზმზე ზემოქმედების გარეშე}.
პროცესი მთავრდება ვირუსული პროტეინებისა და გენომის ე.წ de novo სინთეზით [30].
2.3.3.5 ვირუსული ნაწილაკის აწყობა
ვირუსული გენომისა და ცილების de novo სინთეზის შემდეგ იწყება დაინფიცირებული უჯრედის შიგნით ვირუსული ნაწილაკის აწყობა. ამ სტადიას ასევე უწოდებენ მომწიფების ფაზას (maturation phase) [34]. ამ ეტაპზე უჯრედში მყოფმა ვირუსმა ვირიონის წარმოსაქმნელად, უნდა დაძლიოს ორი ფუნდამენტური პრობლემა. ჯერ-ერთი, მან მხოლოდ გენეტიკურ ინფორმაციაზე დაყრდნობით, შესაბამისი კომპონეტებისგან უნდა ააწყოს ნაწილაკი, რომელიც შემდგომში თავად შექმნის იდენტურ ახალ ნაწილაკს, და მეორე, რაც არანაკლებ რთული ამოცანაა, ამ აწყობილ ნაწილაკს (ვირიონს) უნდა გააჩნდეს მკაცრად დაცული რეგულარული გეომეტრიული ფორმა, მაშინ როდესაც მასალა (ძირითადად ცილის მოლეკულები) რისგანაც ის იწყობა სულაც არ არის რეგულარული ფორმის. ჩნდება კითხვა: როგორ ახერხებენ ეს მარტივი ორგანიზმები ამ სირთულეების დაძლევას? ორივე პრობლემის გადაწყვეტა დაკავშირებულია სიმეტრიისა და ჯგუფთა თეორიასთან [10, 34], რაზეც „მცირე დოზით“ ქვემოთ ვისაუბრებთ.
ხშირად ცალკეული ვირუსული კომპონენტის აწყობა ხორციელდება უჯრედის სხვადასხვა არეში, რომლებსაც მოიხსენიებენ „ვირუსულ ფაბრიკებად“, სადაც დიდი რაოდენობით „იწარმოება“ კაფსიდური ცილები და ვირუსული გენომები. ციტოსკელეტური (Cytoskeleton) კომპონენტები და უჯრედული ორგანელები ხშირად მჭიდრო კავშირშია როგორც აწყობასთან, ისე ვირუსის გამოთავისუფლების პროცესებთან (თუმცა ზოგიერთი უმარტივესი ვირუსის აწყობა (მართალია არაეფექტური) შესაძლებელია კოლბაშიც) [29].
როდესაც ყველა საჭირო „აგური“ (ცილის მოლეკულები) და გენეტიკური მასალა (ვირუსული გენომური ასლები) გამზადებულია, იწყება მკაცრი გეომეტრიული ფორმის მქონე ვირიონის აწყობა „უფორმო აგურებისგან“. სწორედ აქ ერთვება ზემოთ ნახსენები სიმეტრიისა და ჯგუფთა თეორიის მექანიზმი.
ვირუსული ნაწილაკის ასაწყობად, მონომერებს (კაფსომერები), რომლისგან შედგება ვირუსის კაფსიდი, შეუძლიათ თვითაწყობა; გენომის ასლები ცალ-ცალკე უკავშირდება ვირუსულ ცილებს, რათა მოხდეს ყოველი გენომის კაფსომერებთან გაერთიანება. რეპლიცირებული კაფსომერული ცილები დამოუკიდებლად იწყობიან გენომის გარშემო ანუ ქმნიან ნუკლეოკაფსიდს. სხვა საჭირო ცილები ასევე წინასწარ მომზადებულია მასპინძელი უჯრედის მიერ და თვითორგანიზდებიან კაფსიდის სტრუქტურაში (სურ 8).
თვითორგანიზაციის ერთ-ერთი მექანიზმი მდგომარეობს, პროცესის ერთი რომელიმე წვეროდან („საძირკველი“) დაწყებაში და შემდეგ ამ პროცესის თანდათანობით სიმეტრიულად გავრცელებაში. მაგრამ რა განსაზღვრავს „ფასადის“ სიგრძეს, ანუ ორ მოსაზღვრე წვეროს შორის მანძილს, რომელიც განაპირობებს ვირიონის საერთო ზომას? მაგალითად, PRD1 ბაქტერიოფაგის კაფსიდის შექმნისას ეს არის თითქმის ხაზოვანი ფორმის ცილა, შემდგარი 83 ფრაგმენტისგან, რომელიც ასრულებს მოლეკულური სახაზავის როლს, რომელიც ეხმარება ვირუსს გაიზარდოს საჭირო ზომამდე. „მოლეკულური თამაშის მონაწილეები“, რომლებიც ახორციელებენ ამ მექანიზმს ნაჩვენებია სურ.7-ზე. დიმერი შემდგარი ორი ასეთი მოლეკულისგან განსაზღვრავს მანძილებს ბაქტერიოფაგში, რომელსაც აქვს დიამეტრი დაახლოებით 70 ნმ [34,39].

ბევრი მომწიფებული ვირუსი შეიძლება შეიცავდეს დეფექტებს, მათ შორის არასრულ გენომებს და ანომალურ კაფსიდებს. დეფექტური ვირუსების რაოდენობა უმნიშვნელოა ნორმალურ ვირუსების რაოდენობასთან შედარებით, რომლებიც წარმატებით გადადიან ინფექციის ბოლო ეტაპზე [39].
ამრიგად, ვირუსული ქრომოსომის ვირუსულ კაფსიდთან გაერთიანება შეიძლება ჩაითვალოს ვირუსის აწყობის პროცესის კულმინაციად, რაც საბოლოოდ იძლევა ინფექციურ ნაწილაკს (სურ.8) [18-22].
2.3.4.6 ვირუსის გამოთავისუფლება
გამოთავისუფლების ფაზა წარმოადგენს ვირუსის რეპლიკაციის ბოლო სტადიას. სინთეზის სტადიის მსგავსად, ეს ეტაპიც სხვადასხვაგვარად ხორციელდება სხვადასხვა ტიპის ვირუსებში [32-34]. ზოგადად მასპინძელ-უჯრედში აწყობილი ვირიონების მიერ უჯრედის დატოვება ხდება სამი შესაძლო გზიდან ერთ-ერთით, ესენია: ლიზისი (lysis), გამოკვირტვა (budding) და ეკზოციტოზი (exocytosis). ცალკეულ შემთხვევაში ციტოსკელეტა შეიძლება წარმოადგენდეს ბარიერს ახალი ვირიონების გამოსათავისუფლებლად, შესაბამისად ზოგიერთი უგარსო ვირუსი ახდენს ციტოსკელეტის დამშლელი ცილების კოდირებას და ამ ხერხით ათავისუფლებს გზას ახალი ვირიონების უჯრეთგარეთა სივრცეში გამოსაშვებად. [29,33]
ლიზისის გზით დაინფიცირებული უჯრედიდან ვირიონების გამოთავისულებას უმეტესად ახორციელებენ უგარსო და კომპლექსური სტრუქტურის ვირუსები. ამ მიზანს ვირუსები აღწევენ უჯრედის დაპროგრამებით, რასაც თან სდევს ლიზისი – უჯრედის დაშლა და მისი დაღუპვა (იხ.სურ.6 გ)). უჯრედში ლიზისის პროცესის აღძვრა შეიძლება მოხდეს ვირუსული სპეციფიკური ცილებით. უმრავლეს შემთხვევაში დაინფიცირებული უჯრედი ექვემდებარება ლიზის, რამდენადაც ის ნელ-ნელა კვდება ვირუსული ინფექციის განმავლობაში [32,34].
სხვა ტიპის ვირუსები, პირველი შემთხვევისგან განსხვავებით შეიძლება დარჩეს უჯრედში ხანგრძლივი პერიოდის განმავლობაში, გამოთავისუფლების ფაზამდე მიუღწევლად. ზოგიერთ შემთხვევაში ამ დაყოვნებულმა ვირუსებმა შეიძლება გამოიწვიონ უჯრედების სწრაფი გამრავლება და სიმსივნის წარმოშობა. ზოგიერთი სიმსივნე კი შეიძლება გადაიზარდოს კიბოშიც [34,37].
დაინფიცირებული უჯრედიდან გამოთავისუფლების მეორე გზის – გამოკვირტვის შემთხვევაში ნუკლეოკაფსიდი „პოულობს“ შესაფერის „გამოსაკვირტ“ ადგილს. ვირუსი შიგნიდან „მიწოლით“ (ვირუსული გარსის ცილების ციტოპლაზმატური კუდის სფეციფიკური ურთიერთქმედების აღძვრით) გარეთ გამობურცავს უჯრედის ზედაპირს და ეს გამობურცვა გრძელდება მანამ, სანამ თავად არ გაეხვევა უჯრედული მემბრანის ბუშტუკში, შედეგად ის უჯრედის ზედაპირზე აფორმირებს კვირტის მაგვარ გამობურცულობას. {უჯრედული მემბრანებს, რომლებმაც შეიძლება მონაწილეობა მიიღონ გამოკვირტვაში, მიეკუთნება პლაზმური მემბრანა, ენდოსომური და ბირთვული მემბრანები). შემდეგ ეტაპზე ეს კვირტი წყდება უჯრედის მემბრანას და წარმოქმნის გარსით შემოსაზღვრულ ვირუსულ კაფსიდს, რომელიც შედგება უჯრედული მემბრანისა და ვირუსული ცილებისგან (სურ.8). {ვირუსები, რომლებიც გამოიკვირტებიან პლაზმური მემბრანიდან (მაგ აივ ვირუსი), გამოიყოფა ინდივიდუალურად}გარსიანი ვირუსები როგორც წესი, გამოკვირტვას ახდენენ ნელ-ნელა, თანდათანობით, შესაბამისად ასეთ შემთხვევაში უჯრედი ინარჩუნებს სიცოცხლისუნარიანობას, თუმცა ამავე დროს მთელი ამ ხსნის განმავლობაში იწვევს მუდმივ ინფექციას და აქედან გამომდინარე ხანგრძლივ დაავადებას.

ზოგიერთი გარსიანმა ვირუსმა, რომელთა გარსებს აქვთ ენდოსომური ან ბირთვულ მემბრანული წარმომავლობობა, შეიძლება წარმოქმნან ვეზიკულები, რომლებიც შემდგომ ხვდებიან პლაზმურ მემბრანაში და მასთან შერწყმით უჯრეთ გარეთ გამოათავისუფლებენ მასში მოთავსებულ აწყობილ ვირიოენებს, სწორედ ეს პროცესი მოიხსენიება ეკზოციტოზად (სურ.9) [29].

ვირუსულ ინფექციებთან დაკავშირებული დაავადებების უმრავლესობა, ვითარდება უჯრედების ფუნქციის დაკარგვის გამო. ვირუსის რეპლიკაცია ხელს უშლის უჯრედს შეასრულოს თავის ფუნქციები. ამან კი საერთო ჯამში შეიძლება გამოიწვიოს ორგანიზმის დანარჩენი ნაწილის დისფუნქცია. ვირუსებმა, რომლებიც აინფიცირებენ სხეულის მნიშვნელოვანი ორგანოების უჯრედებს, შეიძლება გამოიწვიონ სიკვდილიც. დრო, რომელიც აუცილებელია ვირუსული ინფექციის სიმპტომების გამოსავლენად, დამოკიდებულია მისი რეპლიკაციის სიჩქარეზე. ეს განპირობებულია იმ გარემოებით, რომ ორგანიზმზე, დაინფიცირებული უჯრედების ფუნქციის მოშლით, ზეგავლენის მოსახდენად საჭიროა განსაზღვრული რაოდენობის უჯრედების დაინფიცირება [29,34].
მას შემდეგ რაც ვირიონები გამოთავისუფლდება ისინი მზად არიან დააინფიცირონ როგორც იმავე მასპინძლი-ორგანიზმის ახალი უჯრედები, ასევე სხვა მასპინძელიც და გაიმეორონ რეპლიკაციის იგივე ციკლი (იხ. სურ 9.)[18-22]. ვირიონის მექანიზმის იმდენად ეფექტურობა, რომ ყოველ უჯრედს, რომელსაც დააინფიცირებს თუნდაც ერთი ვირიონი, შეუძლია აწაროოს ასობით ათასი და მეტი ახალი ვირიონი [36]. ასევე საინტერესოა თუ საშუალოდ რამდენი ვირიონის გამოთავისუფლება შეუძლია ერთ ჯერზე დაინფიცირებულ უჯრედს?
დადგენილია რომ ეს რაოდენობა დამოკიდებულია როგორც უჯრედის ტიპზე (პროკარიოტი/ეუკარიოტი, ერთუჯრედიანი/მრავალუჯრედიანი) ისე ვირუსის სახეობაზე და ზომებზე. ასე მაგალითად T1 ბაქტერიოფაქების ე.წ გამოსვლის სიდიდე „burst size“ ≈100-300 [40], ხოლო აივ-ის მსგავსი SIV (Simian Immunodeficiency Virus (SIV)) ვირუსისთვის, რომელიც აინფიცირებს მაინმუნებს და იწვევს მათში შიდსის მსგავს დაავადებას და აინფიცირებს T-უჯრედებს ეს სიდიდე შეადგენს ≈50 000 [41], მაშინ როდესაც ციაბობაქტერიული ვირუსებისთვის ეს სიდიდე შეადგენს ≈ 40-80 [42].
ქვემოთ წარმოდგენილია ვიდეო ანიმაცია ცხოველური ვირუსის უჯრედში შესვლის მექანიზმების შესახებ.
2.3.4 ბაქტერიოფაგების სასიცოცხლო ციკლი პროკარიოტულ მასპინძლებში
ბაქტერიოფაგების სასიცოცხლო ციკლი არის კარგი მოდელი იმის გასაგებად, თუ როგორ ზემოქმედებენ ვირუსები მათ მიერ დაინფიცირებულ უჯრედებზე, რადგან ანალოგური პროცესები დაიმზირება ეუკარიოტული ვირუსებისთვის, რომლებსაც შეუძლიათ გამოიწვიონ უჯრედების დაუყოვნებლივი სიკვდილი ან განაპირობონ ფარული ან ქრონიკული ინფექციები.
ბაქტერიოფაგებმა, რომლებიც აინფიცირებენ ბაქტერიებს, შეიძლება გაიარონ ე.წ ლიზისური ან ლიზოგენური სასიცოცხლო ციკლი, თუმცა არსებობს ცალკეული ვირუსები, რომლებსაც შეუძლიათ ორივე ციკლის განხორციელება [43-48]. განვიხილოთ ისინი უფრო დაწვრილებით.
2.3.4.1 ლიზისური ციკლი
ლიზისურ ციკლში (ამ ციკლს ზოგჯერ მოიხსენიებენ ვირულენტურ ინფექციად), ვირულენტური ფაგები (Virulent phages), სრულად იმორჩილებს მასპინძელ უჯრედს და დაუყოვნებლივ იწყებს რეპლიკაციას, რაც საბოლოო ჯამში მთავრდება ლიზისის შედეგად უჯრედის მოსპობით და ერთბაშად დიდი რაოდენობით ვირუსული ნაწილაკების გამოთავისუფლებით (იხ.სურ 6 გ) [44-45].
Т- ფაგები წარმოადგენენ ვირულენტური ფაგების თვალსაჩინო მაგალითს. გამოყოფენ ბაქტერიოფაგის ლიზსური ციკლის 5 სტადიას (სურ.6 გ)):
- მიმაგრება წარმოადგენს ინფექციის პროცესში პირველ სტადიას, რომლის დროსაც ფაგი ურთიერთქმედებს ბაქტერიული ზედაპირის სპეციფიკურ რექცეპტორებთან (მაგ. ლიპოპოლისაქარიდებთან და OmpC ცილასთან მასპინძლის ზედაპირზე);
- მეორე ეტაპს წარმოადგენს შეღწევა. ეს ხდება კუდის გარსის შემცირების ხარჯზე, რომელიც მოქმედებს როგორც ნემსი თავი ინექციისას, რომლის დროსაც შეჰყავს ვირუსული გენომი უჯრედული კედლის და მემბრანის განჭოლვით. ფაგის თავი და დანარჩენი კომპონენტები რჩება ბაქტერიული უჯრედის გარეთ;
- ინფექციის მესამე ეტაპია – ახალი ვირუსული კომპონენტების ბიოსინთეზი. მასპინძელ უჯრედში მოხვედრის შემდეგ ვირუსი ახორციელებს ფერმენტ ენდონუკლეაზას სინთეზს (რომლის კოდირებასაც თავად ახდენს) ბაქტერიული ქრომოსომის დასაშლელად. ამის შემდეგ ის მთლიანად განკარგავს მასპინძელ-უჯრედს და ამ უკანასკნელს იყენებს ახალი ვირიონის ასაწყობად საჭირო ვირუსული კომპონენტების (კაფსომერების, გარსის, საბაზისო ფირების, კუდის ბოჭკოებისა და ვირუსული ფერმენტების) სინთეზისთვის, მოკლედ რომ ვთქვათ უჯრედს იყენებს რეპლიკაციის, ტრანსკრიპციის და ტრანსლაციისთვის. პოლიმერაზიული გენები ჩვეულებრივ ექსპერირდებიან ციკლის დასაწყისში, მაშინ, როდესაც კაფსიდური და კუდის ცილების ექსპერსია ხდება მოგვიანებით;
- მომწიფების ეტაპზე იქმნება ახალი ვირიონები. იმისათვის, რომ გამოთავისუფლდეს აწყობილი ფაგები, ბაქტერიის უჯრედული კედელი იშლება ფაგის ისეთი ცილების ზემოქმედებით, როგორიცაა ჰოლინი (holin) და ლიზოციმი (lysozyme);
- ბოლო ეტაპია გამოთავისუფლება. მომწიფებული ვირუსები ხეთქავენ მასპინძელი უჯრედის კედელს ლიზისისას. შთამომავალი ვირიონები გამითავისუფლდებიან გარემოში ახალი უჯრედების დასაინფიცირებლად [44,48].
- ქვემოთ წარმოდგენილია ვიდეო ანიმაცია.
ქვემოთ წარმოდგენილია ვიდეო ანიმაცია ბაქტერიოფაგის უჯრედის შეღწევაზე.
2.3.4.2 ლიზოგენური ციკლი
ლიზოგენური ციკლი, რომელსაც ასევე მოიხსენიებენ ზომიერ ან არავირულენტურ ინფექციად, ლიზიურისგან განსხვავებით არ იწვევს მასპინძელი უჯრედის ლიზისს მაშინათვე. ზომიერი ფაგები (Temperate phages) მასპინძელ უჯრედს იყენებს თავშესაფარად, სადაც ვირუსი იმყოფება უმოქმედო (ლატენტურ) ფაზაში [43-45].
ლიზოგენური ციკლის დროს ვირუსის მიერ მასპინძელ უჯრედში გენეტიკური მასალის შეყვანის (ინექციის) შემდეგ, ვირუსული გენომი, მის მიერვე კოდირებადი ფერმენტის ინტეგრაზას (Integrase) მეშვეობით ჩაინერგება მასპინძლის დნმ-ში ან წარმოქმნის წრიულ რეპლიკონს (replicon) ბაქტერიულ ციტოპლაზმაში. ამ ფაზაში ვირუსი უმოქმედოა და არ არის საზიანო მასპინძლისთვის, ამ მდგომარეობაში მას მოიხსენიებენ პროფაგად (ზოგან ხმარობენ ტერმინს – ენდოგენური ფაგები (endogenous phage)). პროფაგის გენომი მასპინძლის გენომთან ერთად პასიურად რეპლიცირდება და მასპინძელ უჯრედის გამრავლების კვალდაკვალ თავადაც მრავლდება (იხ. სურ.10) [43-47].

2.3.4.3 ლიზოგენური ციკლიდან ლიზისურში გადასვლა
მასპინძელი უჯრედისა და პროფაგის მშვიდობიანი თანაცხოვრება გრძელდება მანამ, სანამ მასპინძლის მდგომარეობა არ გაუარესდება, რაც შეიძლება გამოიხატოს, საკვები ნივთიერებების ამოწურვით ან სტრესორების, ისეთების როგორიცაა ულტრაიისფერი გამოსხივება, ქიმიური ნივთიერების ზემოქმედებით (მაგალითად მიტომიცინ C (mitomycin C)). ასეთ შემთხვევაში პროფაგები ხდება აქტიური, კერძოდ, მას შეუძლია თავისთავადად გამოეყოს მასპინძლის გენომს და გადაერთოს ლიზისურ ციკლზე, რომელსაც ასევე უწოდებენ ინდუქციურ პროცეს (სურათი 10)[43-45]. ეს პროცესი, არ არის იდეალური, პროფაგმა შეიძლება ცალკეულ შემთხვევებში მასპინძელი უჯრედის გენომიდან თავისი გენომის გამოყოფისას (ამოღებისას) დატოვოს თავისი დნმ-ს ფრაგმენტი ან პირიქით „გადმოაყოლოს“ მასპინძლის დნმ-ს ფრაგმენტი. თუ ასეთი ფაგები კვლავ დააინფიცირებენ ახალ მასპინძელ-უჯრედს, მათ შეიძლება გადაიტანონ ბაქტერიული გენები ერთი შტამიდან მეორეზე რასაც ეწოდება ტრანსდუქცია (იხ. ნაწილი I) [45].
ქვემოთ წარმოდგენილია ვიდეო ანიმაცია ლიზისურ და ლიზოგენური ციკლების შორის განსხვავებაზე.
2.3.5 ლატენტური პერიოდი
ვირუსები, რომლებიც აინფიცირებენ მცენარეების ან ცხოველების უჯრედებს, შეიძლება თვითონვე დაექვემდებარონ ინფექციას, როდესაც ისინი თავად არ ახორციელებენ საკუთარი ვირიონების წარმოქმნას დიდი ხნის განმავლობაში. მაგალითად გამოდგება ცხოველების ჰერპესის ვირუსები, მათ შორის მარტივი ჰერპესისი ვირუსი, რომელიც იწვევს ორალურ და გენიტალურ ჰერპესს ადამიანეში. ლატენტურ (უმოქმედო) პროცესში, ეს ვირუსები შეიძლება არსებობდნენ ნერვულ უჯრედებში ძალიან დიდი ხნის განმავლობაში ახალი ვირიონების წარმოქმნის გარეშე, მხოლოდ პერიოდულად გამოდიან ლატენტური ფაზიდან და იწვევენ კანის დაზიანებას, რომლის დროსაც ვირუსი მრავლდება. მიუხედავად იმისა, რომ არსებობს ლიზგოგენურობასა და ლატენტობას შორის მსგავსება, ტერმინი ლიზოგენური ციკლი ჩვეულებრივ გამოიყენება ბაქტერიოფაგების სასიცოცხლო ციკლის აღსაწერად.
2.3.6 ვირუსული ინფექციის ეტაპები
როგორც ზემოთ ავღნიშნეთ, ვირუსმა თვითწარმოქმნისთვის უნდა გამოიყენოს უჯრედული პროცესები. ვირუსის რეპლიკაციის ციკლმა მასპინძელი-უჯრედში შეიძლება გამოიწვიოს დრამატული ბიოქიმიური და სტრუქტურული ცვლილებები. ასეთი სახის ცვლილებებს უწოდებენ ციტოპათიკურ (Cytopathic effect) ეფექტს და მან შეიძლება გამოიწვიოს უჯრედის ფუნქციის შეცვლა (მოშლა) და დაღუპვაც კი [33]. მაგალითად გაციების ერთ-ერთი ვირუსით – რინოვირუსით დაინფიცირებული ზოგიერთი უჯრედი, იღუპება ლიზისის ან აპოპტოზის („უჯრედების თვითმკვლელობა“) გამო. ვირუსული დაავადების სიმპტომები წარმოადგენს იმუნური სისტემის პასუხს ვირუსზე – რომელიც ცდილობს დაამყაროს კონტროლი უჯრედზე. იმუნური სისტემის მოვალეობაა გამოიყვანოს ვირუსი ორგანიზმიდან და აღმოფხვრას მის მიერ გამოწვეულ უჯრედულ დაზიანებები. მწვავე ვირუსულ დაავადებებისთვის დამახასიათებელია სიმპტომების გამწვავება მოკლე პერიოდში, რის შემდეგაც იმუნურ სისტემას გამოჰყავს ვირუსი ორგანიზმიდან ინფექციისგან შესაძლო გამოჯანმრთელების შედეგით. მწვავე ვირუსული დაავადებების მაგალითს წარმოადგენს გაციება და გრიპი.
მრავალი ცხოველური ვირუსი, ისეთი როგორიცაა, აივ-ი, იმუნური სისტემის ინფიცირებულ უჯრედებს ტოვებს ე.წ გამოკვირტვის პროცესის მეშვეობით, რომლის დროსაც ვირიონები უჯრედებს ტოვებენ ინდივიდუალურად. ამ პროცესის დროს მართალია არ ხდება უჯრედის ლიზისი და ის არ იღუპება მაშინათვე, თუმცა იმ უჯრედულმა დაზიანებებმა, რომელიც გამოიწვია ვირუსით დაინფიცირებამ, შეიძლება მოშალოს ამ უკანასკნელის ნორმალური ფუნქციონირება, მიუხედავად იმისა, რომ უჯრედები ცოცხალია გარკვეული პერიოდის განმავლობაში[30,33].
ზოგიერთი ვირუსი იწვევს ხანგრძლივ ქრონიკულ ინფექციებს, მაგალითად С ჰეპატიტის გამომწვევი ვირუსი, ზოგი კი, ისეთები როგორიცაა მარტივი ჰერპესის ვირუსი, იწვევს მხოლოდ პერიოდულ სიმპტომებს. ცალკეულმა ვირუსებმა (მაგალითად ადამიანის მე-6 და მე-7 ტიპის ჰერპესვირუსი), პაციენტებში შეიძლება საერთოდ არ გამოიწვიოს არანაირი სიმპტომები.
გამოყენებული ლიტერატურა:
- Gregory A. C., Zayed A. A., Conceição-Neto N., Temperton B., Bolduc B., Alberti A., … Cruaud, C. (2019). Marine DNA Viral Macro- and Microdiversity from Pole to Pole. Cell. doi:10.1016/j.cell.2019.03.040
- Shuttle C.A. Marine viruses — major players in the global ecosystem. Nature Reviews Microbiology, 5(10), 801–812. 2007, DOI:10.1038/nrmicro1750
- https://www.ncbi.nlm.nih.gov/books/NBK209710/
- https://ucmp.berkeley.edu/bacteria/bacterialh.html
- https://www.krugosvet.ru/enc/nauka_i_tehnika/biologiya/BAKTERII.html
- Whitman WB, Coleman DC, Wiebe WJ. Prokaryotes: the unseen majority. Proc Natl Acad Sci U S A. 1998;95(12):6578–6583. DOI: 10.1073/pnas.95.12.6578
- Beijerinck M.W., On a Contagium vivum fluidum causing the Spotdisease of the Tobacco-leaves, in: KNAW, Proceedings, 1, 1898-1899, Amsterdam, 1899, pp. 170-176
- https://courses.lumenlearning.com/microbiology/chapter/viruses/
- On the historical significance of Beijerinck and his contagium vivum fluidum for modern virology. HPLS 40, 41 (2018). https://doi.org/10.1007/s40656-018-0206-1
- 318 pages, 2015 ISBN: 0128019468 გვ.3
- Forterre P., The origin of viruses and their possible roles in major evolutionary transitions. Virus Research, 117(1), 5–16. (2006). DOI:10.1016/j.virusres.2006.01.010
- Koonin EV, Senkevich TG, Dolja VV. The ancient Virus World and evolution of cells. Biol Direct. 2006; 1:29. Published 2006 Sep 19. DOI:10.1186/1745-6150-1-29
- https://www.webmd.com/a-to-z-guides/qa/how-do-viruses-differ-from-bacteria
- https://www.sciencealert.com/virus
- https://www.virology.ws/2010/07/22/the-virus-and-the-virion/
- https://www.nature.com/scitable/topicpage/the-origins-of-viruses-14398218/
- https://studfile.net/preview/4666820/page:7/
- B.W.J., Marc H.V. van Regenmortel, Desk Encyclopedia of General Virology, — Boston: Academic Press, 2010. გვ.167. pp.663 ISBN: 978-0-12-375146-1
- https://www.differencebetween.com/difference-between-virus-and-vs-virion/
- https://www.differencebetween.com/difference-between-obligate-intracellular-parasite-and-vs-bacteriophage/#Obligate%20Intracellular%20Parasite
- http://www.opentextbooks.org.hk/ditatopic/35518
- https://www.drugs.com/medical-answers/difference-between-bacteria-virus-3503840/
- Mahmoudabadi G, Phillips R. A comprehensive and quantitative exploration of thousands of viral genomes. Elife. 2018;7:e31955. DOI: 10.7554/eLife.31955
- King Andrew M.Q., Lefkowitz E., Adams M.J., Casrstens E, B., Virus Taxonomy: Ninth Report of the International Committee on Taxonomy of Viruses, ISBN: 978-0-12-384684-6 (2011) Elsevier, (p.3) p. 1272.
- https://www.virology.ws/2009/08/12/simplifying-virus-classification-the-baltimore-system/
- https://byjus.com/biology/virus/
- Venkataram Prasad BV, Schmid MF. Principles of virus structural organization. Adv Exp Med Biol. 2012;726:17‐47. DOI:10.1007/978-1-4614-0980-9_3.
- Sattley W Matthew, Madigan, Michael T (August 2015) Microbiology. In: eLS. John Wiley & Sons, Ltd: Chichester. https://doi.org/10.1002/9780470015902.a0000459.pub2
- Payne Susan, Viruses From Understanding to Investigation, Department of Veterinary Medicine and Biomedical Sciences, Texas A&M University, College Station, Texas, United States, 2017, Pages 23-35; https://www.sciencedirect.com/science/article/pii/B9780128031094000039#f0010
- https://www.immunology.org/public-information/bitesized-immunology/pathogens-and-disease/virus-replication
- Dyakov, Y. T., & Zinovyeva, S. V. (2007). Plant parasite microorganisms. Comprehensive and Molecular Phytopathology, 19–47. DOI:10.1016/b978-044452132-3/50004-3
- Hunt M., Virology – chapter two – Basic virology: replication of viruses, Department of Pathology, Microbiology and Immunology, University of South Carolina School of Medicine, https://www.microbiologybook.org/mhunt/replicat.htm
- https://courses.lumenlearning.com/boundless-biology/chapter/virus-infections-and-hosts/
- Aseeri B., Abahussain R., Al-mushawah S., Al-samih N., Alruji N., Rubella Virus (German measles), King Saud University College of Science, https://fac.ksu.edu.sa/sites/default/files/rubella_virus.pdf
- შალიშა ა. სტენლი უჯრედული ბიოლოგია ბიოტექნოლოგებისათვის. (ადაპტირებული თარგმანი, ე. ჩერქეზია), თბილისის სახელმწიფო უნივერსიტეტი, ISBN 978-9941-0-5809-7, 221 გვ. 2013
- Cohen FS. How Viruses Invade Cells. Biophys J. 2016;110(5):1028‐1032. DOI: 10.1016/j.bpj.2016.02.006
- https://www.cancerquest.org/cancer-biology/viruses-and-cancer
- https://viralzone.expasy.org/956?outline=all_by_protein
- http://book.bionumbers.org/how-big-are-viruses/
- Demerec M, Fano U. Bacteriophage-Resistant Mutants in Escherichia Coli. Genetics. 1945 Mar30 (2):119-36. & Delbrük M. Bacterial viruses or bacteriophages. Biol Rev Camb Philos Soc. 1946 PubMed ID17247150, 21016941
- Chen HY, Di Mascio M, Perelson AS, Ho DD, Zhang L. Determination of virus burst size in vivo using a single-cycle SIV in rhesus macaques. Proc Natl Acad Sci U S A. 2007 Nov 27 104(48):19079-84 DOI:10.1073/pnas.0707449104 http://book.bionumbers.org/how-many-virions-result-from-a-single-viral-infection/
- Brown C.M., J. E., & Campbell, D. A. (2006). Are phytoplankton population density maxima predictable through analysis of host and viral genomic DNA content? Journal of the Marine Biological Association of the UK, 86(03), 491. DOI:10.1017/s0025315406013397
- Neil A. Campbell, Jane B. Reece. Biology. San Francisco: Pearson. pp. 337–339. ISBN: 0-321-27045-2
- https://courses.lumenlearning.com/boundless-biology/chapter/virus-infections-and-hosts/
- Steward K. Lytic vs Lysogenic – Understanding Bacteriophage Life Cycles, 2018 https://www.technologynetworks.com/immunology/articles/lytic-vs-lysogenic-understanding-bacteriophage-life-cycles-308094
- Yarmolinsky MB, Hansen EB, Jafri S, Chattoraj DK. Participation of the lytic replicon in bacteriophage P1 plasmid maintenance. J Bacteriol. 1989;171(9):4785‐4791. DOI:10.1128/jb.171.9.4785-4791.1989
- Aman, Bogdan & Ciobanu, Gabriel. (2011). Mutual mobile membranes with objects on surface. Natural Computing. 10. 777-793. 10.1007/s11047-011-9249-x.
- Vander Elst, Niels & Meyer, Evelyne. (2018). Potential therapeutic application of bacteriophages and phage-derived endolysins as alternative treatment of bovine mastitis. Vlaams Diergeneeskundig Tijdschrift. 87. 181-186. 10.21825/vdt.v87i4.16065.